题目内容
向紫色石蕊溶液中加入过量的Na2O2粉末,振荡,下列叙述正确的是( )
| A、溶液仍为紫色 |
| B、最后溶液变为蓝色 |
| C、最后溶液褪色 |
| D、无气泡产生 |
考点:钠的重要化合物
专题:几种重要的金属及其化合物
分析:过氧化钠与水反应生成NaOH和氧气,并且Na2O2具有强氧化性,能使紫色溶液褪色.
解答:
解:过氧化钠与水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑,溶液中有气泡产生,过氧化钠过量,且有强氧化性,能使紫色石蕊溶液因氧化而褪色,溶液最终变为无色.
故选C.
故选C.
点评:本题考查过氧化钠的性质,题目难度不大,注意过氧化钠能使紫色溶液褪色的性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
根据元素周期律判断,下列元素原子半径最小的是( )
| A、Cl | B、S | C、Na | D、Mg |
某有机物的结构简式为: ,则此有机物可发生的反应类型有( )
,则此有机物可发生的反应类型有( )
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦加聚 ⑧中和.
 ,则此有机物可发生的反应类型有( )
,则此有机物可发生的反应类型有( )①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦加聚 ⑧中和.
| A、①②④⑤⑥⑦⑧ |
| B、②③④⑤⑥⑧ |
| C、②③④⑤⑥⑦⑧ |
| D、①②③④⑤⑥⑦⑧ |
下列实验操作均要用到玻璃棒:①过滤;②蒸发;③溶解;④向容量瓶里转移液体,其中玻璃棒的作用相同的是( )
| A、①和② | B、①和③ |
| C、③和④ | D、①和④ |
将下列各组物质按酸、碱、盐分类顺次排列.正确的是( )
| A、硫酸,纯碱,孔雀石 |
| B、硝酸,烧碱,石灰石 |
| C、冰醋酸,乙醇,醋酸钠 |
| D、盐酸,熟石灰,苛性钠 |
水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O32-+O2+xOH-=Fe3O4+S4O62-+2H2O,下列说法中不正确的是( )
| A、每生成1mol Fe3O4,反应转移的电子总数为4mol | ||
| B、Fe2+和S2O32-都是还原剂 | ||
C、1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为
| ||
| D、x=4 |
下列叙述中正确的是( )
| A、物质的量就是物质的质量 |
| B、物质的量就是物质的数量 |
| C、物质的量就是摩尔 |
| D、物质的量的单位是摩尔 |
X、Y、Z、R、Q为元素周期表前20号的五种主族元素,且原子半径依次减小,其中X和Q同主族,X与Z、Y与Q原子的电子层数都相差2,X、Y原子最外层电子数之比为1:4,Z的最外层电子数是次外层的3倍.下列说法不正确的是( )
| A、Y和Z形成的某种化合物具有空间网状结构 |
| B、X和Z可形成X2Z、X2Z2的化合物 |
| C、R和Q形成的化合物含有共价键且为强电解质 |
| D、X的失电子能力比Q强 |
已知HCl气体极易溶于水.下列操作中正确的是( )
A、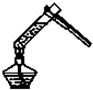 |
B、 |
C、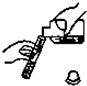 |
D、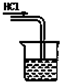 |