题目内容
6. 近年来AIST报告正在研制一种“高容量、低成本”的锂一铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )
近年来AIST报告正在研制一种“高容量、低成本”的锂一铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )| A. | 放电时,Li+透过同体电解质向Cu极移 | |
| B. | 放电时,正极的电极反应式为O2+2H2O+4e-=4OH- | |
| C. | 通空气时,铜被腐蚀,表面产生Cu2O | |
| D. | 通空气时,整个反应过程中,铜相当于是催化剂 |
分析 放电时,锂失电子作负极,Cu上O2得电子作正极,负极上电极反应式为Li-e-═Li+,正极上电极反应式为O2+4e-+2H2O=4OH-,电解质溶液中阳离子向正极移动,阴离子向负极移动,据此分析解答.
解答 解:A.因为原电池放电时,阳离子移向正极,所以Li+透过固体电解质向Cu极移动,故A正确;
B.该电池通过一种复杂的铜腐蚀而产生电力,由方程式可知铜电极上并非是氧气直接放电,正极反应为Cu2O+H2O+2e-=Cu+2OH-,故B错误;
C.放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,可知通空气时,铜被腐蚀,表面产生Cu2O,故C正确;
D.由B项分析知:铜先与氧气反应生成Cu2O,放电时Cu2O重新生成Cu,则整个反应过程中,铜相当于催化剂,故D正确;
故选B.
点评 本题考查了原电池原理,明确原电池负极上得失电子及电极反应式是解本题关键,题目难度中等,注意把握Cu在整个过程中的作用.

练习册系列答案
相关题目
2.下列有关乙烯的说法中错误的是( )
| A. | 乙烯分子中所有原子在同一平面内 | |
| B. | 乙烯分子中含有的官能团是碳碳双键 | |
| C. | 乙烯在一定条件下能与水发生加成反应得到乙醇 | |
| D. | 乙烯能使酸性KMnO4溶液褪色,是因为发生了加成反应 |
3.下列说法正确的是( )
| A. | 升高NH4Cl溶液的温度,其水的离子积常数和pH均增大 | |
| B. | 在有AgI沉淀的上层清液中滴加一定浓度的NaCl溶液,不可能产生白色沉淀 | |
| C. | pH=3的盐酸与pH=11的氨水等体积混合后,溶液中:c(NH4+>c(Cl-)>c(OH-)>c(H+) | |
| D. | 室温下,稀释0.1mol•L-1CH3COOH溶液,溶液的导电能力增强 |
14.某化学兴趣小组从香料中提取下列四种有机物成分,有关说法正确的是( )


| A. | ①②③④均可与Na、NaOH、H2发生反应,1mol四种物质最多消耗Na、NaOH、H2的物质的量之比依次分别为1:1:1:1、1:2:2:1、4:3:3:5 | |
| B. | ①②③④属同分异构体,分子式为C8H8O3 | |
| C. | 可用银氨溶液或酸性KMnO4溶液区分③④ | |
| D. | ①②③④中所有原子均不可能处于同一平面 |
1.下列溶液中各微粒的浓度关系不正确的是( )
| A. | 0.1 mol•L-1的HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) | |
| B. | 等浓度、等体积的Na2CO3和NaHCO3混合:$\frac{c(HC{O}_{3}^{-})}{c({H}_{2}C{O}_{3})}$>$\frac{c(C{O}_{3}^{2-})}{c(HC{O}_{3}^{-})}$ | |
| C. | 0.1 mol•L-1的NaHCO3溶液中:c(Na+)+c(H+)=c(HCO${\;}_{3}^{-}$)+2c(CO${\;}_{3}^{2-}$)+c(OH-) | |
| D. | 等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
11. 含氮有机物对乙酰氨基酚(如图)是生活中常见感冒药的主要成分,下列有关对乙酰氨基酚的说法正确的是( )
含氮有机物对乙酰氨基酚(如图)是生活中常见感冒药的主要成分,下列有关对乙酰氨基酚的说法正确的是( )
 含氮有机物对乙酰氨基酚(如图)是生活中常见感冒药的主要成分,下列有关对乙酰氨基酚的说法正确的是( )
含氮有机物对乙酰氨基酚(如图)是生活中常见感冒药的主要成分,下列有关对乙酰氨基酚的说法正确的是( )| A. | 对乙酰氨基酚的分子式为:C8H10NO2 | |
| B. | 对乙酰氨基酚可与浓溴水发生加成反应 | |
| C. | 与对乙酰氨基酚互为同分异构体,分子中含有硝基和苯环,且苯环上有三个取代基的分子共有6种 | |
| D. | 对乙酰氨基酚可以与Na2CO3发生反应,产生CO2气体 |
18.固体硝酸盐加热易分解且产物较复杂.某学习小组以AgNO3为研究对象,拟通过实验探究其热分解的产物,提出如下3种猜想:
甲:Ag2O、NO2、O2乙:Ag、NO2、O2 丙:Ag2O、NO2、N2
(1)实验前,小组成员经讨论认定猜想丙不成立,理由是不符合氧化还原反应原理.
查阅资料得知:
2NO2+2NaOH═NaNO3+NaNO2+H2O;Ag2O与粉末态的Ag均为黑色;Ag2O可溶于氨水.针对甲、乙猜想,设计如图所示的实验装置(图中加热、夹持仪器等均省略):

(2)实验过程
①仪器连接后,放入固体试剂之前,首先进行的操作是检验装置的气密性.
②将AgNO3固体置于A中,加热前通入N2以驱尽装置内的空气,其目的是避免对产物O2检验产生干扰;关闭K,用酒精灯加热时,正确操作是先移动酒精灯预热硬质玻璃管,然后固定在管中固体部位下加热.
③观察到A 中有红棕色气体出现,C、D 中有气泡.
④待样品完全分解,A 装置冷却至室温.
⑤取少量剩余固体于试管中,加入适量水,未见明显现象.
(3)实验结果分析讨论
①证明一定有O2生成的依据是C中的溶液不褪色,且D中的溶液褪色,与此相关的化学原理为Na2SO3+H2O?NaHSO3+NaOH、2Na2SO3+O2═2Na2SO4(用化学方程式表示).
②针对试管中残留黑色固体的成分,该学习小组进行了如下探究:
【提出假设】试管中残留的黑色固体可能是:ⅰ.Ag;ⅱ.Ag2O;ⅲ.Ag和Ag2O.
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验.
【实验评价】根据上述实验,不能确定固体产物成分的实验是b(填实验编号).
【实验结论】根据上述实验结果,该小组得出AgNO3固体热分解的化学方程式为2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑.
(4)从实验安全的角度判断该实验装置有无缺陷?若有,应如何改进?有,应在AB装置间增加防倒吸的装置.
甲:Ag2O、NO2、O2乙:Ag、NO2、O2 丙:Ag2O、NO2、N2
(1)实验前,小组成员经讨论认定猜想丙不成立,理由是不符合氧化还原反应原理.
查阅资料得知:
2NO2+2NaOH═NaNO3+NaNO2+H2O;Ag2O与粉末态的Ag均为黑色;Ag2O可溶于氨水.针对甲、乙猜想,设计如图所示的实验装置(图中加热、夹持仪器等均省略):

(2)实验过程
①仪器连接后,放入固体试剂之前,首先进行的操作是检验装置的气密性.
②将AgNO3固体置于A中,加热前通入N2以驱尽装置内的空气,其目的是避免对产物O2检验产生干扰;关闭K,用酒精灯加热时,正确操作是先移动酒精灯预热硬质玻璃管,然后固定在管中固体部位下加热.
③观察到A 中有红棕色气体出现,C、D 中有气泡.
④待样品完全分解,A 装置冷却至室温.
⑤取少量剩余固体于试管中,加入适量水,未见明显现象.
(3)实验结果分析讨论
①证明一定有O2生成的依据是C中的溶液不褪色,且D中的溶液褪色,与此相关的化学原理为Na2SO3+H2O?NaHSO3+NaOH、2Na2SO3+O2═2Na2SO4(用化学方程式表示).
②针对试管中残留黑色固体的成分,该学习小组进行了如下探究:
【提出假设】试管中残留的黑色固体可能是:ⅰ.Ag;ⅱ.Ag2O;ⅲ.Ag和Ag2O.
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验.
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
【实验结论】根据上述实验结果,该小组得出AgNO3固体热分解的化学方程式为2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑.
(4)从实验安全的角度判断该实验装置有无缺陷?若有,应如何改进?有,应在AB装置间增加防倒吸的装置.
15.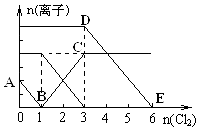 已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.横、纵坐标的单位均为mol.有关说法不正确的是( )
已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.横、纵坐标的单位均为mol.有关说法不正确的是( )
 已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.横、纵坐标的单位均为mol.有关说法不正确的是( )
已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.横、纵坐标的单位均为mol.有关说法不正确的是( )| A. | 线段BC代表Fe3+ 物质的量的变化情况 | |
| B. | 原混合溶液中c(FeBr2)=6 mol/L | |
| C. | 当通入Cl22mol时,溶液中已发生的反应可表示为2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| D. | 原溶液中n (Fe2+):n (I-):n(Br-)=2:1:3 |
19.苯甲酸粗品中含有泥沙和杂质 A(随温度变化 A 的溶解度变化很小),可通过系列操 作完成苯甲酸的提纯.则下列叙述正确的是( )
| A. | 苯甲酸易溶于水,可做食品防腐剂 | |
| B. | 提纯苯甲酸的过程中需要用到的玻璃仪器:烧杯、玻璃棒、漏斗 | |
| C. | 粗品中苯甲酸溶解后,还需再加入少量蒸馏水,以减少产品的损失 | |
| D. | 为了获得更多的苯甲酸,此实验中结晶温度越低越好 |