题目内容
(1)已知:N2(g)+O2(g)=2NO(g);△H=180.5KJ?mol-l
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905KJ?mol-l
2H2(g)+O2(g)=2H2O(g);△H=-483.6KJ?mol-l
则 N2(g)+3H2(g)?2NH3(g)的△H=
(2)一定温度下在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g)?4NO2(g)+O2(g);△H>O
①反应达到平衡后若再通入一定量氮气,则N2O5的转化率将
②下表为反应在T,温度下的部分实验数据:
则500s内N2O5的分解速率为
③在T2温度下,反应1000s时测得NO2的浓度为4.98mol?L-1,则T2
(3)如图所示装置可用于制备N2O5,则N2O5在电解池的
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905KJ?mol-l
2H2(g)+O2(g)=2H2O(g);△H=-483.6KJ?mol-l
则 N2(g)+3H2(g)?2NH3(g)的△H=
-92.4KJ/mol
-92.4KJ/mol
.(2)一定温度下在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g)?4NO2(g)+O2(g);△H>O
①反应达到平衡后若再通入一定量氮气,则N2O5的转化率将
不变
不变
(填“增大”、“减小”、“不变”).②下表为反应在T,温度下的部分实验数据:
| 时间/S | 0 | 500 | 1000 |
| c(N2O5)mol?L-1 | 5.00 | 3.52 | 2.48 |
2.96×10-3mol/L?S
2.96×10-3mol/L?S
.③在T2温度下,反应1000s时测得NO2的浓度为4.98mol?L-1,则T2
<
<
T1.
(3)如图所示装置可用于制备N2O5,则N2O5在电解池的
阳
阳
(填“阳极”或“阴极”)区生成,其电极反应式为N2H4+2HNO3-2e-=2N2O5+2H+
N2H4+2HNO3-2e-=2N2O5+2H+
.分析:(1)依据热化学方程式和盖斯定律概念分析计算得到;
(2)①一定温度下在恒容密闭容器中通入惰气总压增大分压不变,平衡不动;
②依据化学反应速率是利用单位时间物质浓度变化计算得到;
③2N2O5(g)?4NO2(g)+O2(g);△H>O,反应是吸热反应,反应的N2O5浓度变化=5.00-2.48=2.52mol/L,二氧化氮浓度为5.04mol/L,在T2温度下,反应1000s时测得NO2的浓度为4.98mol?L-1,二氧化氮浓度减小,平衡逆向进行,说明温度降低;
(3)由N2O4制取N2O5需要是去电子,所以N2O5在阳极区生成.
(2)①一定温度下在恒容密闭容器中通入惰气总压增大分压不变,平衡不动;
②依据化学反应速率是利用单位时间物质浓度变化计算得到;
③2N2O5(g)?4NO2(g)+O2(g);△H>O,反应是吸热反应,反应的N2O5浓度变化=5.00-2.48=2.52mol/L,二氧化氮浓度为5.04mol/L,在T2温度下,反应1000s时测得NO2的浓度为4.98mol?L-1,二氧化氮浓度减小,平衡逆向进行,说明温度降低;
(3)由N2O4制取N2O5需要是去电子,所以N2O5在阳极区生成.
解答:解:(1)①N2(g)+O2(g)=2NO(g);△H=180.5KJ?mol-l
②4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905KJ?mol-l
③2H2(g)+O2(g)=2H2O(g);△H=-483.6KJ?mol-l
依据盖斯定律计算得到,N2(g)+3H2(g)?2NH3(g)的△H=-184.8KJ/mol;
则N2(g)+3H2(g)?2NH3(g)的△H=-92.4KJ/mol;
故答案为:-92.4KJ/mol;
(2)①一定温度下在恒容密闭容器中通入惰气总压增大分压不变,平衡不动,则N2O5的转化率不变,故答案为:不变;
②500s内N2O5的分解速率=
=2.96×10-3mol/L?S;
故答案为:2.96×10-3mol/L?S;
③2N2O5(g)?4NO2(g)+O2(g);△H>O,反应是吸热反应,反应的N2O5浓度变化=5.00-2.48=2.52mol/L,二氧化氮浓度为5.04mol/L,在T2温度下,反应1000s时测得NO2的浓度为4.98mol?L-1,二氧化氮浓度减小,平衡逆向进行,说明温度降低,T2<T1;
故答案为:<;
(3)从电解原理来看,N2O4制备N2O5为氧化反应,则N2O5应在阳极区生成,反应式为N2O4+2HNO3-2e-=2N2O5+2H+,
故答案为:阳极,N2O4+2HNO3-2e-=2N2O5+2H+.
②4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905KJ?mol-l
③2H2(g)+O2(g)=2H2O(g);△H=-483.6KJ?mol-l
依据盖斯定律计算得到,N2(g)+3H2(g)?2NH3(g)的△H=-184.8KJ/mol;
则N2(g)+3H2(g)?2NH3(g)的△H=-92.4KJ/mol;
故答案为:-92.4KJ/mol;
(2)①一定温度下在恒容密闭容器中通入惰气总压增大分压不变,平衡不动,则N2O5的转化率不变,故答案为:不变;
②500s内N2O5的分解速率=
| 5.00mol/L-3.52mol/L |
| 500S |
故答案为:2.96×10-3mol/L?S;
③2N2O5(g)?4NO2(g)+O2(g);△H>O,反应是吸热反应,反应的N2O5浓度变化=5.00-2.48=2.52mol/L,二氧化氮浓度为5.04mol/L,在T2温度下,反应1000s时测得NO2的浓度为4.98mol?L-1,二氧化氮浓度减小,平衡逆向进行,说明温度降低,T2<T1;
故答案为:<;
(3)从电解原理来看,N2O4制备N2O5为氧化反应,则N2O5应在阳极区生成,反应式为N2O4+2HNO3-2e-=2N2O5+2H+,
故答案为:阳极,N2O4+2HNO3-2e-=2N2O5+2H+.
点评:本题考查了热化学方程式和盖斯定律的计算应用化学平衡影响因素的分析判断,电解原理的分析应用,速率计算和平衡移动原理的应用是解题关键,题目难度中等.

练习册系列答案
相关题目
 利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题: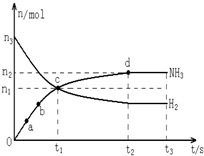 自1913年工业合成氨投产以来,合成氨工业不断发展,氨又可以进一步制备硝酸,在工业上可进行连续生产.请回答下列问题:
自1913年工业合成氨投产以来,合成氨工业不断发展,氨又可以进一步制备硝酸,在工业上可进行连续生产.请回答下列问题:

