题目内容
为测定某K2SO4溶液的浓度,取50.00mL待测液,向其中加入过量的BaCl2溶液,充分反应后过滤并干燥,得到BaSO4沉淀2.33克.该K2SO4溶液的物质的量浓度是多少?
考点:化学方程式的有关计算
专题:
分析:发生反应K2SO4+BaCl2═BaSO4↓+2KCl,根据n=
计算硫酸钡物质的量,根据方程式可知n(K2SO4)=n(BaSO4),再根据c=
计算c(K2SO4).
| m |
| M |
| n |
| V |
解答:
解:233g硫酸钡的物质的量为
=0.01mol,
由K2SO4+BaCl2═BaSO4↓+2KCl,n(K2SO4)=n(BaSO4)=0.01mol,
则c(K2SO4)=
=0.2mol/L
答:该K2SO4溶液的物质的量浓度是0.2mol/L.
| 2.33g |
| 233g/mol |
由K2SO4+BaCl2═BaSO4↓+2KCl,n(K2SO4)=n(BaSO4)=0.01mol,
则c(K2SO4)=
| 0.01mol |
| 0.05L |
答:该K2SO4溶液的物质的量浓度是0.2mol/L.
点评:本题考查化学方程式有关计算,比较基础,侧重对基础知识的巩固.

练习册系列答案
相关题目
图中E表示反应物或生成物的能量,下列说法正确的是( )


| A、图1可表示C+O2→CO2的能量变化过程 |
| B、图1可表示CaCO3→CaO+CO2的能量变化过程 |
| C、图2可表示Mg+2HCl→MgCl2+H2 的能量变化过程 |
| D、图1表示的反应是吸热反应,图2表示的反应是放热反应 |
在下列有关晶体的叙述中错误的是( )
| A、液态水的密度比冰的密度大,因为水中氢键多 |
| B、原子晶体中,只存在共价键 |
| C、各类晶体中,只有分子晶体才存在分子 |
| D、稀有气体的原子能形成分子晶体 |
CO、O2、CO2混合气体9mL,点燃爆炸后,恢复到原状况下,体积减少1mL,再通过足量浓NaOH溶液时,体积又减少5mL(体积均在相同状况下测定),则原混合气体中CO、O2、CO2的体积比为( )
| A、1:3:5 |
| B、5:1:3 |
| C、2:4:3 |
| D、3:1:5 |
某优质甜樱桃中含有一种羟基酸(用M表示),M的碳链结构无支链,分子式为C4H6O5;1.34g M与足量的碳酸氢钠溶液反应,生成标准状况下的气体0.448L.M在一定条件下可发生如下转化:M
A
B
C(M、A、B、C分子中碳原子数目相同).下列有关说法中不正确的是( )
| 浓硫酸 |
| △ |
| Br2 |
| 足量NaOH溶液 |
| A、M的结构简式为HOOC-CH(OH)-CH2-COOH |
| B、B能发生酯化、消去、取代等反应 |
| C、与M官能团种类、数量完全相同的同分异构体还有2种 |
| D、C物质不可能溶于水 |
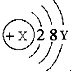 ,试回答:
,试回答: