题目内容
20.(1)书写下列反应的离子方程式.①氢氧化铜和稀盐酸溶液:Cu(OH)2+2H+=2H2O+Cu2+.
②氢氧化钡溶液与硫酸溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O.
③碳酸氢钠溶液和硫酸氢钠溶液:HCO3-+H+=H2O+CO2↑.
④向足量澄清石灰水中通入二氧化碳Ca2++2OH-+CO2=CaCO3↓+H2O
(2)用双线桥法表示下列氧化还原反应中电子转移的方向和数目.
4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
分析 (1)①氢氧化铜与盐酸反应生成氯化铜和水;
②氢氧化钡溶液与稀硫酸反应生成硫酸钡沉淀和水;
③碳酸氢钠与硫酸氢钠反应生成硫酸钠、二氧化碳气体和水;
④二氧化碳少量,反应生成碳酸钙沉淀和水;
(2)氨气分子中N元素化合价从-3变为0价,氧气中O元素化合价从0价变为-2价,据此用双线桥法表示该氧化还原反应中电子转移的方向和数目.
解答 解:(1)①氢氧化铜不溶于水,离子方程式中应写成化学式,反应的离子方程式为:Cu(OH)2+2H+=2H2O+Cu2+,
故答案为:Cu(OH)2+2H+=2H2O+Cu2+;
②氢氧化钡溶液与硫酸溶液反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,
故答案为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;
③碳酸氢钠溶液与硫酸氢钠溶液反应的离子反应为:HCO3-+H+=H2O+CO2↑,
故答案为:HCO3-+H+=H2O+CO2↑;
④二者反应生成碳酸钙和水,离子反应为:Ca2++2OH-+CO2=CaCO3↓+H2O,
故答案为:Ca2++2OH-+CO2=CaCO3↓+H2O;
(2)NH3失去6个电子变成N2,O2得到6个电子变成H2O,用双线桥法表示该氧化还原反应中电子转移的方向和数目为: ,
,
故答案为: .
.
点评 本题考查了氧化还原反应中电子转移的表示方法、离子方程式的书写,题目难度中等,明确氧化还原反应的表示方法为解答关键,注意掌握离子方程式的书写原则,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
10.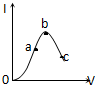 在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示,下列叙述正确的是( )
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示,下列叙述正确的是( )
 在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示,下列叙述正确的是( )
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示,下列叙述正确的是( )| A. | a、b、c三点处,溶液c(H+)由小到大的顺序为a、b、c | |
| B. | a、b、c三点处,电离程度最大的是b | |
| C. | a、b、c三点处,c(CH3COO-)最大的是c | |
| D. | 若使c点溶液中c(CH3COO-)增大,可采取的措施有加入NaOH固体或加热 |
11.某溶液由Mg2+、Al3+、Cl-、SO${\;}_{4}^{2-}$4种离子组成,测得其中Al3+、SO${\;}_{4}^{2-}$、Cl-的物质的量浓度之比为3:1:13,则溶液中Mg2+、Al3+、SO${\;}_{4}^{2-}$的物质的量浓度之比为( )
| A. | 1:3:3 | B. | 3:1:3 | C. | 3:3:1 | D. | 2:1:3 |
8.下列叙述正确的是( )
| A. | pH=2的硫酸溶液中c(H+):c(OH-)等于2:1,稀释100倍后二者的比值几乎不变 | |
| B. | 由水电离的c(H+)=10-12mol/L的溶液中:K+、Ba2+、Cl-、Br-、一定能大量共存 | |
| C. | 1.0×10-3mol/L盐酸溶液的pH=3,则1.0×10-8mol/L盐酸溶液的pH=8 | |
| D. | 某温度下水的离子积为1.0×10-12,若使pH=1的H2SO4溶液与pH=12的NaOH溶液混合后溶液呈中性,则两者的体积比为10:1 |
5.下列变化中,需要加入还原剂才能实现的是( )
| A. | Cl-→Cl2 | B. | H2→H+ | C. | CuO→Cu | D. | Zn→Zn2+ |
10.某有机物结构简式为 ,下列叙述不正确的是( )
,下列叙述不正确的是( )
 ,下列叙述不正确的是( )
,下列叙述不正确的是( )| A. | 1mol该有机物在加热和催化剂作用下,最多能和4 molH2反应 | |
| B. | 该有机物能使溴水褪色也能使酸性KMnO4溶液褪色 | |
| C. | 该有机物属于烃 | |
| D. | 该有机物在一定条件下,能发生消去反应或取代反应 |