题目内容
16. 如图是制取、洗涤并测量生成气体体积的装置示意图,利用该装置进行下表所列实验,能达到实验目的是( )
如图是制取、洗涤并测量生成气体体积的装置示意图,利用该装置进行下表所列实验,能达到实验目的是( )物质 实验 | a(液体) | b(固体) | c(液体) |
| A | 稀硫酸 | 锌粒 | 浓H2SO4 |
| B | 稀硫酸 | 石灰石 | 浓H2SO4 |
| C | 浓硫酸 | Cu片 | NaOH溶液 |
| D | 稀HNO3 | Cu片 | H2O |
| A. | A | B. | B | C. | C | D. | D |
分析 由实验装置可知,分液漏斗中的液体与烧瓶中固体发生反应、且不需要加热,c为除杂装置,最后为排水法测定气体的体积,则气体不溶于水,以此来解答.
解答 解:A.Zn与稀硫酸反应生成氢气,浓硫酸干燥氢气,氢气不溶于水,可排水法测定氢气的体积,故A选;
B.石灰石与稀硫酸反应生成硫酸钙微溶,包裹在石灰石的表面,阻止反应的发生,不能制备气体,故B不选;
C.Cu与浓硫酸反应需要加热,故C不选;
D.Cu与稀硝酸反应生成NO,NO不溶于水,可排水法测定NO的体积,故D选;
故选AD.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、气体的制备原理、实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意元素化合物与实验的结合,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.将漂白粉配成溶液晾置在空气中,过了一段时间,其漂白效果会更好的原因可能是( )
| A. | 漂白粉被氧化了 | |
| B. | 有色布条被空气中的氧气氧化了 | |
| C. | 漂白粉跟空气中的 CO2反应充分,生成了较多量的 HClO | |
| D. | 漂白粉溶液蒸发掉部分水,其浓度增大 |
1.下列说法正确的是( )
| A. | 食用白糖的主要成分是蔗糖 | |
| B. | 油脂、淀粉和蛋白质都是高分子化合物 | |
| C. | 油脂不能使溴水褪色 | |
| D. | 乙酸乙酯和食用油都可以水解生成乙醇 |
8.下列关于氢键说法不正确的是( )
| A. | 常温时水呈液态是因为水分子间可以形成氢键 | |
| B. | NH3易溶于水的原因之一是它与水分子间能形成氢键因为能形成氢键 | |
| C. | H2O比H2S稳定是因为水分子间可以形成氢键,而H2S不能 | |
| D. | 乙醇可以与水互溶是因为它与水分子间可以形成氢键 |
5.可逆反应:2A+2B?C+3D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是( )
| A. | v(A)=0.0075 mol•L-1•min-1 | B. | v(B)=0.01 mol•L-1•mim-1 | ||
| C. | v(C)=0.5 mol•L-1•s-1 | D. | v(D)=0.4 mol•L-1•s-1 |
6.下列说法错误的是( )
| A. | HF可以用于刻蚀玻璃 | |
| B. | 用小苏打(NaHCO3)发酵面团制作馒头 | |
| C. | SO2具有漂白性,可用于漂白纸浆,也可以大量用于漂白食品 | |
| D. | 纯碱用于生产普通玻璃,也可用纯碱溶液来除去物品表面的油污 |
 (I)由短周期元素构成的A~E五种物质中都含有同一种元素,B为单质.
(I)由短周期元素构成的A~E五种物质中都含有同一种元素,B为单质. ,A既能与强酸又能与强碱反应,且都能产生气体,请画出A的电子式为
,A既能与强酸又能与强碱反应,且都能产生气体,请画出A的电子式为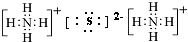 或
或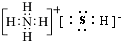 .
.