题目内容
13.设NA表示阿伏加德罗常数的值,下列说法错误的是( )| A. | 若1mol•L-1HF溶液中H+数目为NA,则等体积的2mol•L-1HF溶液中H+数目为2NA | |
| B. | 44gCO2、N2O组成的混合气体中所含有的原子数为3NA | |
| C. | 36g3H2中含有的中子数目为24NA | |
| D. | 2.24L(标准状况)O2与钠反应时,转移电子数目可能为0.3NA |
分析 A、HF为弱酸,浓度越大,则电离程度越小;
B、CO2、N2O的摩尔质量均为44g/mol,且均为三原子分子;
C、求出3H2的物质的量,然后根据1mol3H2中含4mol中子来分析;
D、氧气反应后的价态可能为-1价,也可能为-2价.
解答 解:A、HF为弱酸,浓度越大,则电离程度越小,故若1mol•L-1HF溶液中H+数目为NA,则等体积的2mol•L-1HF溶液中H+数目小于2NA,故A错误;
B、CO2、N2O的摩尔质量均为44g/mol,故44g混合物的物质的量为1mol,且两者均为三原子分子,故1mol混合物中含3NA个原子,故B正确;
C、36g3H2的物质的量为n=$\frac{36g}{6g/mol}$=6mol,而1mol3H2中含4mol中子,故6mol3H2中含24NA个中子,故C正确;
D、标况下2.24L氧气的物质的量为0.1mol,而氧气反应后的价态可能为-1价,也可能为-2价,故0.1mol氧气当全部变为-1价时转移0.2NA个电子,当全部变为-2价时转移0.4NA个电子,由于产物中氧元素的价态不明确,故转移的电子介于0.2NA到0.4NA之间,即可能为0.3NA个,故D正确.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.短周期主族元素A、B、C、D的原子序数依次增大,A、C的原子序数的差为8,A原子最外层电子数是其次外层电子数的3倍,B原子在同周期主族元素中的原子半径最大.下列说法正确的是( )
| A. | 原子半径:r(C)<r(D)<r(B) | |
| B. | 元素A与B只能形成一种化合物 | |
| C. | A的简单气态氢化物的热稳定性比C的强 | |
| D. | C的最高价氧化物的水化物的酸性比D的强 |
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1mol对苯二甲酸中含有双键的数目为0.2NA | |
| B. | 常温下,1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| C. | Fe在少量Cl2中燃烧生成0.5 mol产物,转移的电子数为NA | |
| D. | 标准状况下,2.24L H2S全部溶于水所得溶液中HS-和S2-离子数之和为0.1NA |
8.锌银电池在放电时,电池总反应方程式可表示为:Zn+Ag2O+H2O=Zn(OH)2+2Ag.下列有关化学电池的说法正确的是( )
| A. | 该电池又称纽扣电池,是可充电池,适用于大电流连续放电 | |
| B. | 该电池属于碱性电池,放电过程中,锌失去电子生成锌离子,向负极移动 | |
| C. | 该电池在放电过程中,正极的pH变大 | |
| D. | 该电池的负极反应式:Zn-2e-=Zn2+ |
18.在标准状况下,下列物质中含氢原子数最多的是( )
| A. | 3g H2 | B. | 11.2L HCl | C. | 1.12L H2O | D. | 3.01×1023个CH4 |
5.下列说法正确的是( )
| A. | 分子晶体中,可能不存在共价键,但一定存在分子间作用力 | |
| B. | 两种元素组成的分子中一定只有极性键 | |
| C. | 只含共价键的物质,一定是共价化合物 | |
| D. | 氧化还原反应中,一种元素化合价上升,一定有另一种元素化合价下降 |
2.在8.08g铁与铜的混和物中,加入200mL、0.6mol/L的稀硝酸,充分反应后剩余金属5.44g,再向其中加入50mL、0.4mol/L的稀硫酸,充分振荡后剩余金属4.48g.若硝酸的还原产物只有NO,下列说法正确的是( )
| A. | 剩余的5.44g金属为铁 | B. | 剩余5.44g金属为铜 | ||
| C. | 共生成NO气体 0.03mol | D. | 8.08g金属中铁的质量分数为20.8% |
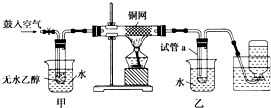 某实验小组用下列装置进行乙醇催化氧化的实验.
某实验小组用下列装置进行乙醇催化氧化的实验.