题目内容
4.下述实验设计合理的是( )| A. | 用锌粒和稀硝酸反应制备H2 | B. | 用NH4NO3加热制取NH3 | ||
| C. | 大理石与稀硫酸反应制备CO2 | D. | 用焰色反应鉴别固体NaCl和 KCl |
分析 A.稀硝酸有强氧化性,生成一氧化氮;
B.NH4NO3受热易爆炸;
C.大理石与稀硫酸反应生成硫酸钙微溶物;
D.Na和K元素的焰色反应现象不同.
解答 解:A.稀硝酸有强氧化性,生成一氧化氮,不生成氢气,故A错误;
B.NH4NO3受热易爆炸,应用氯化铵和氢氧化钙制取氨气,故B错误;
C.大理石与稀硫酸反应生成硫酸钙微溶物,阻止反应进一步进行,故C错误;
D.Na和K元素的焰色反应现象不同,可将二者鉴别,故D正确.
故选D.
点评 本题综合考查化学实验方案的评价,侧重于物质的检验和制备的考查,题目难度不大,注意把握相关实验的注意事项以及相关物质的性质.

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
14.下列物质中既能脱水生成烯烃又能催化氧化生成醛的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
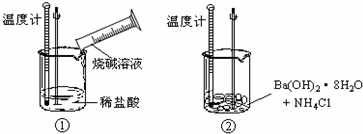
12.下列化学反应既是氧化还原反应,又是反应物总能量低于生成物总能量的是( )
| A. | 甲烷在氧气中的燃烧反应 | B. | 铝与稀盐酸的反应 | ||
| C. | Ba(OH)2•8H2O与NH4Cl的反应 | D. | 灼热的碳与二氧化碳的反应 |
19.判断下列各组物质,互为同系物的是( )
| A. | C2H6和C4H10 | B. | C3H8和C5H10 | C. | C6H6和C6H12 | D. | CH4和C2H2 |
9.用图中装置进行实验,实验一段时间后,现象与预测不一致的是( )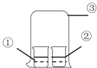

| ①中物质 | ②中物质 | 实验预测 | |
| A | 浓氨水 | 酚酞试液 | ②中溶液变为红色 |
| B | 浓硝酸 | 淀粉KI溶液 | ②中溶液变为蓝色 |
| C | 浓盐酸 | 浓氨水 | 大烧杯中有白烟 |
| D | 饱和的亚硫酸溶液 | 稀溴水 | ②中无明显变化 |
| A. | A | B. | B | C. | C | D. | D |
7.1mol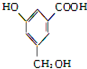 分别与NaHCO3、Na、NaOH反应消耗掉的三者的物质的量之比为( )
分别与NaHCO3、Na、NaOH反应消耗掉的三者的物质的量之比为( )
 分别与NaHCO3、Na、NaOH反应消耗掉的三者的物质的量之比为( )
分别与NaHCO3、Na、NaOH反应消耗掉的三者的物质的量之比为( )| A. | 1:1:1 | B. | 1:3:2 | C. | 2:3:1 | D. | 1:2:3 |
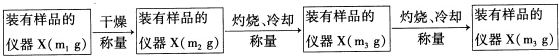
 .
. .
. .
.