题目内容
18.某有机物结构式为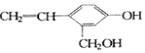 ,它不可能具有的性质是( )
,它不可能具有的性质是( )①可以燃烧 ②能使酸性高锰酸钾溶液褪色 ③能跟KOH溶液反应 ④能发生聚合反应 ⑤能发生消去反应 ⑥能与金属钠反应 ⑦能发生取代反应 ⑧能被氧化.
| A. | ⑤ | B. | ①②③④⑥⑦⑧ | C. | ①⑤⑦ | D. | ⑤⑧ |
分析 由结构可知,分子中含碳碳双键、酚-OH、醇-OH,结合烯烃、醇、酚的性质来解答.
解答 解:为烃的含氧衍生物,可燃烧生成二氧化碳和水;
含碳碳双键,能使酸性高锰酸钾溶液褪色,能发生聚合反应,能被氧化;
含酚-OH,具有酸性,能跟KOH溶液反应,能与金属钠反应,能发生取代反应,能被氧化;
含-OH,能使酸性高锰酸钾溶液褪色,能与金属钠反应,能发生取代反应,能被氧化,与-OH相连C的邻位C上无H,不能发生消去反应,
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意消去反应的结构特点,题目难度不大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
19.在下列情况下,物质不能导电的是( )
| A. | 熔化的硝酸钾 | B. | 硝酸钾晶体 | C. | 硝酸钾水溶液 | D. | 稀盐酸 |
9.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生.下列属于未来新能源标准的是( )
①太阳能 ②核能 ③煤 ④氢能 ⑤地热能 ⑥天然气 ⑦风能 ⑧石油.
①太阳能 ②核能 ③煤 ④氢能 ⑤地热能 ⑥天然气 ⑦风能 ⑧石油.
| A. | ④⑤⑥⑦⑧ | B. | ①②⑤⑦⑧ | C. | ②③⑥⑦⑧ | D. | ①②④⑤⑦ |
6. 已知NaCl的摩尔质量为Mg•mol-1,食盐晶体的密度为ρ•cm-3,若图中N+与邻近的C-的核间距离为acm,那么阿伏加德罗常数的值表示为( )
已知NaCl的摩尔质量为Mg•mol-1,食盐晶体的密度为ρ•cm-3,若图中N+与邻近的C-的核间距离为acm,那么阿伏加德罗常数的值表示为( )
 已知NaCl的摩尔质量为Mg•mol-1,食盐晶体的密度为ρ•cm-3,若图中N+与邻近的C-的核间距离为acm,那么阿伏加德罗常数的值表示为( )
已知NaCl的摩尔质量为Mg•mol-1,食盐晶体的密度为ρ•cm-3,若图中N+与邻近的C-的核间距离为acm,那么阿伏加德罗常数的值表示为( )| A. | 2Ma3ρ | B. | $\frac{M}{{a}^{3}ρ}$ | C. | $\frac{2M}{{a}^{3}ρ}$ | D. | $\frac{M}{2{a}^{3}ρ}$ |
13.下列各组物质中,互为同系物的是( )
| A. | CH3-CH=CH2和  | |
| B. |  和 和  | |
| C. |  和 和 | |
| D. | CH2=CH-CH=CH2和CH3-CH2-CH2-C≡CH |
3.氰氨基化钙是一种重要的化工原料,其制备的化学方程式为:CaCO3+2HCN=CaCN2+CO↑+H2↑+CO2↑,下列说法正确的是( )
| A. | CO为氧化产物,H2为还原产物 | B. | CaCN2中含有非极性键 | ||
| C. | HCN既是氧化剂又是还原剂 | D. | 每消耗10g CaCO3生成2.24L CO2 |
10.关于下列图示的说法中,正确的是( )
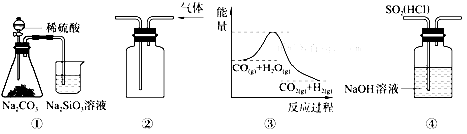

| A. | 图①所示实验可比较硫、碳、硅三种元素的非金属性强弱 | |
| B. | 用图②所示实验装置排空气法收集CO2气体 | |
| C. | 图③表示可逆反应CO(g)+H 2O (g)?CO2(g)+H2(g) 是吸热反应 | |
| D. | 图④装置可以用来除去SO2中的HCl |
7.下列物质或物质的主要成分对应化学式错误的是( )
| A. | 胆矾(CuSO4•5H2O) | B. | 磁性氧化铁(Fe3O4) | C. | 苏打(NaHCO3) | D. | 铁锈(Fe2O3•xH2O) |
12. 电解质溶液电导率越大导电能力越强.常温下用0.100mol•L-1盐酸分别滴定10.00mL浓度均为0.100mol•L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氮相似,常温Kb[(CH3)2NH]=1.6×10-4.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法正确的是( )
电解质溶液电导率越大导电能力越强.常温下用0.100mol•L-1盐酸分别滴定10.00mL浓度均为0.100mol•L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氮相似,常温Kb[(CH3)2NH]=1.6×10-4.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法正确的是( )
 电解质溶液电导率越大导电能力越强.常温下用0.100mol•L-1盐酸分别滴定10.00mL浓度均为0.100mol•L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氮相似,常温Kb[(CH3)2NH]=1.6×10-4.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法正确的是( )
电解质溶液电导率越大导电能力越强.常温下用0.100mol•L-1盐酸分别滴定10.00mL浓度均为0.100mol•L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氮相似,常温Kb[(CH3)2NH]=1.6×10-4.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法正确的是( )| A. | 曲线②代表滴定二甲胺溶液的曲线 | |
| B. | A点溶液中:c(H+)=c(OH-)+c[(CH3)2NH•H2O] | |
| C. | D点溶液中:2c(Na+)=3c(Cl-) | |
| D. | 在相同温度下,A、B、C、D四点的溶液中,水的电离程度最大的是C点 |