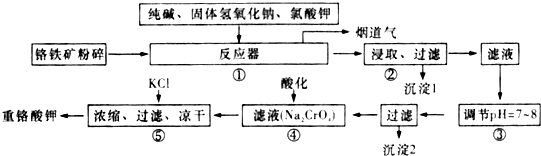
题目内容
15. 已知:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素.其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;G原子核外价电子数与B相同,其余各层均充满.B、E两元素组成化合物B2E的晶体为离子晶体.C、F的原子均有三个能层,C原子的第一至第四电离能(KJ•mol-1)分别为578、1 817、2 745、11 575;C与F能形成原子数目比为1:3、熔点为190℃的化合物Q.
已知:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素.其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;G原子核外价电子数与B相同,其余各层均充满.B、E两元素组成化合物B2E的晶体为离子晶体.C、F的原子均有三个能层,C原子的第一至第四电离能(KJ•mol-1)分别为578、1 817、2 745、11 575;C与F能形成原子数目比为1:3、熔点为190℃的化合物Q.(1)B的单质晶体为体心立方堆积模型,其配位数为8;E元素的最高价氧化物分子的立体构型是平面三角形.F元素原子的核外电子排布式是1s22s22p63s23p5,G的高价离子与A的简单氢化物形成的配离子的化学式为[Cu(NH3)4]2+.
(2)试比较B、D分别与F形成的化合物的熔点高低并说明理由NaCl的熔点高于SiCl4,因为NaCl是离子晶体,SiCl4是分子晶体.
(3)A、G形成某种化合物的晶胞结构如图所示.若阿伏加德罗常数为NA,该化合物晶体的密度为a g•cm-3,其晶胞的边长为$\root{3}{{\frac{206}{{a{N_A}}}}}$ cm.
(4)在1.01×105 Pa、T1℃时,气体摩尔体积为53.4L•mol-1,实验测得Q的气态密度为5.00g•L-1,则此时Q的组成为Al2Cl6.
分析 A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素,A原子在基态时p轨道半充满且电负性是同族元素中最大的,则A为第VA族元素,同一主族元素中,元素的电负性随着原子序数的增大而减小,所以A为N元素;
D、E原子核外的M层中均有两个未成对电子,E的原子序数大于D,D、E外围电子排布分别为3s23p2,3s23p4,所以D为Si元素、E为S元素;
B、E两元素组成化合物B2E的晶体为离子晶体,说明B为活泼金属,B为+1价,B的原子序数大于A小于D,所以B为Na元素;
C、F的原子均有三个能层,为第三周期元素,C原子第三电离能剧增,则最外层电子数为3,故C为Al,C与F能形成原子数目比为1:3、熔点为190℃的化合物Q,故G为Cl;
G原子核外最外层电子数与B相同,G最外层电子数是1,其余各层均充满,则G元素的核电荷数=2+8+18+1=29,为Cu元素.
解答 解:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素,A原子在基态时p轨道半充满且电负性是同族元素中最大的,则A为第VA族元素,同一主族元素中,元素的电负性随着原子序数的增大而减小,所以A为N元素;
D、E原子核外的M层中均有两个未成对电子,E的原子序数大于D,D、E外围电子排布分别为3s23p2,3s23p4,所以D为Si元素、E为S元素;
B、E两元素组成化合物B2E的晶体为离子晶体,说明B为活泼金属,B为+1价,B的原子序数大于A小于D,所以B为Na元素;
C、F的原子均有三个能层,为第三周期元素,C原子第三电离能剧增,则最外层电子数为3,故C为Al,C与F能形成原子数目比为1:3、熔点为190℃的化合物Q,故G为Cl;
G原子核外最外层电子数与B相同,G最外层电子数是1,其余各层均充满,则G元素的核电荷数=2+8+18+1=29,为Cu元素.
(1)Na的单质晶体为体心立方堆积模型,8个顶点上各有一个原子,体心上含有一个原子,所以其配位数为8;E元素的最高价氧化物为SO3,三氧化硫分子中价层电子对个数是3且不含孤电子对,所以三氧化硫分子的立体构型是平面三角形;F是Cl元素,原子核外有17个电子,根据构造原理知,F元素原子的核外电子排布式是1s22s22p63s23p5;G的高价离子与A的简单氢化物形成的配离子为铜氨络离子,铜氨络离子的化学式为[Cu(NH3)4]2+,
故答案为:8;平面三角形;1s22s22p63s23p5;[Cu(NH3)4]2+;
(2)B和E形成的化合物是氯化钠,D和E形成的化合物是四氯化硅,氯化钠为离子晶体,四氯化硅为分子晶体,一般来说,离子晶体的熔点大于分子晶体,所以氯化钠的熔点高于四氯化硅,
故答案为:NaCl的熔点高于SiCl4,因为NaCl是离子晶体,SiCl4是分子晶体;
(3)A为N元素,G为Cu元素,该晶胞中,Cu原子个数=12×$\frac{1}{4}$=3,N原子个数=8×$\frac{1}{8}$=1,该晶胞的化学式为Cu3N,该晶胞的边长=$\root{3}{{\frac{m}{ρ}}}$=$\root{3}{{\frac{{\frac{206}{N_A}}}{a}}}$cm=$\root{3}{{\frac{206}{{a{N_A}}}}}$cm,
故答案为:$\root{3}{{\frac{206}{{a{N_A}}}}}$;
(4)Q的摩尔质量=ρVm=5.00g/L×53.4L/mol=267g/mol,AlCl3的摩尔质量为133.5g/mol,Q的摩尔质量是氯化铝的2倍,所以Q分子中含有2个铝原子和6个氯原子,其化学式为Al2Cl6,
故答案为:Al2Cl6.
点评 本题考查了物质结构与性质,涉及核外电子排布、元素周期律、空间构型判断、晶体类型与性质、晶胞的计算等,正确推断元素是解本题关键,掌握均摊法进行晶胞的有关计算.

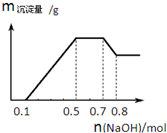 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味无毒的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉 淀的物质的量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味无毒的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉 淀的物质的量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )| A. | 溶液中的阳离子只有H+、NH4+、Mg2+、Al3+ | |
| B. | 溶液中n(NH4+)=0.1mol | |
| C. | 溶液中一定不含CO32-,可能含有SO42-和NO3- | |
| D. | 三种离子的物质的量之比n(H+):n(Al3+):n(Mg2+)=1:1:1 |
| A. | 钠在实验室通常保存在煤油中,可推知锂也可保存在煤油中 | |
| B. | FeCl2与Cl2反应生成FeCl3,可推知FeBr2也可与Br2反应生成FeBr3 | |
| C. | 工业制Mg采用电解MgCl2的方法,可推知工业制Al也采用电解AlCl3的方法 | |
| D. | CO2通入Ba(NO3)2溶液中无明显现象,可推知SO2通入Ba(NO3)2溶液中也无明显现象 |
| A. | 2HA+C3-═2A-+H2C- | B. | H3C+3A-═3HA+C3- | ||
| C. | H3C+B2-═HB-+H2C- | D. | HB-+A-═HA+B2- |
| A. | 船舶防腐时,船体上加装的阳极锌需定期更换 | |
| B. | 合成氨反应中使用高效催化剂可提高原料转化率 | |
| C. | 将图中的活塞快速推至A处固定,气体颜色先变深、再变浅,但比起始时深 | |
| D. | 等体积、等浓度NaOH溶液和CH3COOH溶液混合后溶液pH=7 |
 ClO2是一种国际上公认的安全无毒的绿色水处理剂.回答下列问题:
ClO2是一种国际上公认的安全无毒的绿色水处理剂.回答下列问题: