题目内容
12.下列变化过程中,没有发生化学变化的是( )| A. | 铝的钝化 | B. | 光合作用 | C. | 碘的升华 | D. | 海水提溴 |
分析 A.铝钝化生成三氧化二铝;
B.光合作用过程中有新物质氧气等生成;
C.碘的升华没有新物质生成;
D.海水提溴有新物质溴生成.
解答 解:A.铝钝化生成三氧化二铝,有新物质生成,属于化学变化,故A错误;
B.光合作用过程中有新物质氧气等生成,属于化学变化,故B错误;
C.碘的升华没有新物质生成,属于物理变化,故C正确;
D.海水提溴有新物质溴生成,属于化学变化,故D错误.
故选C.
点评 本题考查物理变化与化学变化的区别与联系,难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列反应中生成物总能量高于反应物总能量的是( )
| A. | 盐酸与NaOH溶液反应 | B. | 碳酸氢铵受热分解 | ||
| C. | 铝粉与MnO2反应 | D. | 氧化钙溶于水 |
3.下列各溶液中,有关微粒的物质的量浓度的叙述正确的是( )
| A. | 25℃时,NH4Cl与NH3•H2O混合溶液中:c(C1-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 将pH=3的醋酸溶液稀释后,溶液中所有离子的浓度均降低 | |
| C. | 将pH=2 HCl与pH=12 NH3•H2O溶液等体积混合,混合后溶液中c(H+)=c(OH-) | |
| D. | 0.01mol•L-1Na2CO3溶液与0.01mol•L-1NaHCO3溶液等体积混合一定存在:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+) |
20.下列有关化学用语表示正确的是( )
| A. | 羟基的电子式: | B. | 乙炔的结构式:CHCH | ||
| C. | 硝基苯的结构简式: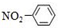 | D. | 甲烷分子的球棍模型: |
7.硅酸钠的水溶液俗称“水玻璃”,是建筑行业经常使用的一种黏合剂.硅酸钠属于( )
| A. | 盐 | B. | 氧化物 | C. | 碱 | D. | 酸 |
17.下列有关物质用途的说法不正确的是( )
| A. | 碳铵与碱性肥料混合施用.以提高肥效 | |
| B. | 用氧化铝制造耐火材料 | |
| C. | 在医疗上,可用碳酸氢钠治疗胃酸过多 | |
| D. | 用硫酸钡制作白色颜料 |
4.如图装置可处理乙醛废水,乙醛在阴、阳极分别转化为乙醇和乙酸.下列说法正确的是( )

| A. | b电极为正极 | |
| B. | 电解过程中,阴极区Na2SO4的物质的量增大 | |
| C. | 阳极电极反应式为CH3CHO-2e-+H2O═CH3COOH+2H+ | |
| D. | 电解过程中,阴、阳极还分别产生少量的O2和H2 |
1.下列离子方程式正确且能解释事实的是( )
| A. | 氯气常用于饮用水消毒:Cl2+H2O?HClO+H++Cl- | |
| B. | 用漂白精溶液吸收尾气的SO2:Ca2++ClO-+SO2+H2O═CaSO3↓+2HClO | |
| C. | 铝离子、亚铁离子开始沉淀的pH分别是4.1、7.5,在Al2Fe(SO4)4溶液中滴加少量烧碱溶液产生白色沉淀:Fe2++20H-=Fe(OH)3↓ | |
| D. | 用银为电极电解盐酸:2H++2Cl-$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑ |
16.高氯酸铵(NH4ClO4)和铝粉常用作火箭推进剂的固体燃料.高温时,NH4ClO4的分解反应是:2NH4ClO4$\frac{\underline{\;高温\;}}{\;}$ N2↑+4H2O↑+Cl2↑+2O2↑下列有关NH4ClO4的分解及保存方法说法不合理的是( )
| A. | 点燃铝粉可以引发NH4ClO4分解 | |
| B. | NH4ClO4迅速分解时可能会引发爆炸 | |
| C. | NH4ClO4应低温通风保存,远离火种、热源 | |
| D. | 0.5 mol NH4ClO4分解时产生的气体体积是44.8 L |