题目内容
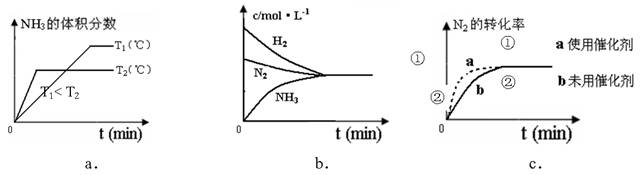
在一定条件下,对于密闭容器中进行的可逆反应:N2(g)+3H2(g)?2NH3(g),下列说法中,能说明该反应已经达到化学平衡状态的是( )
| A.N2、H2、NH3在密闭容器中共存 |
| B.N2、H2、NH3的浓度不再变化 |
| C.N2、H2、NH3的浓度相等 |
| D.正、逆反应速率都等于零 |
A、反该反应为可逆反应,无论是否达到平衡状态,各种物质都共存,故A错误;
B、因达到平衡时,正逆反应速率相等,各种物质的浓度不再发生变化,故B正确;
C、因反应平衡时各物质的浓度不变,但不是说各自的浓度相等,故C错误;
D、因反应达到平衡时,正逆反应速率相等,但反应并没有停止,故D正确;
故选:B.
B、因达到平衡时,正逆反应速率相等,各种物质的浓度不再发生变化,故B正确;
C、因反应平衡时各物质的浓度不变,但不是说各自的浓度相等,故C错误;
D、因反应达到平衡时,正逆反应速率相等,但反应并没有停止,故D正确;
故选:B.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
将E和F加入固定容积的密闭容器中,在一定条件下发生反应:
E(g)+F(s)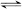 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
|
压强/MPa 体积分数/% 温度/℃ |
1.0 |
2.0 |
3.0 |
|
810 |
54.0 |
a |
b |
|
915 |
c |
75.0 |
d |
|
1000 |
e |
f |
83.0 |
(1)915℃、2.0MPa时E的转化率为 。
(2)该反应的△S 0(填“>”、“<”或“=”,下同),b f。
(3)平衡常数K(1000℃) K(810℃) ,理由是 。
(4)对于上述反应,下列说法正确的是 (填序号)。
①混合气体的密度不再变化,反应达到平衡
②该反应的正反应为放热反应
③增大F的量,单位体积活化分子数增大,化学反应速率加快
④恒温恒容条件下通入惰性气体,平衡不移动
⑤恒温恒压条件下通入惰性气体,化学反应速率加快
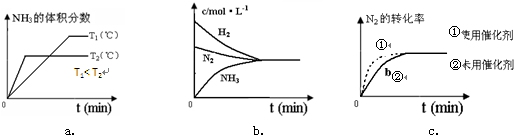
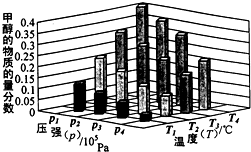 能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚. 2NH3(g) △H=" -92.4KJ/mol " ,据此回答以下问题:
2NH3(g) △H=" -92.4KJ/mol " ,据此回答以下问题: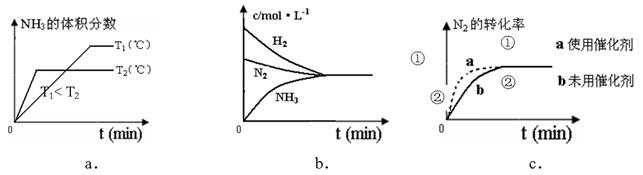
 2NH3(g) △H= -92.4KJ/mol ,据此回答以下问题:
2NH3(g) △H= -92.4KJ/mol ,据此回答以下问题: