题目内容
某课外活动小组设计了如图所示(夹持装置已略去)的一套装置,用H2和CuO冶炼Cu。准确称取3.180 g CuO放在硬质玻璃管内.已知:CuO—黑色、Cu2O—红色、Cu—红色。
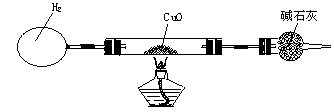
试通过计算回答[①气体体积按标准状况计,②Ar(Cu)=63.5,Ar(O)=16.0,Ar(H)=1.00]:
(1)下列H2球较适合用于本实验的是__________(填选项编号)
A.500 mL H2 球 B.896 mL H2 球 C.1500 mL H2 球
(2)反应至黑色全部变为红色止,测量H2球的体积变为220 mL,固体质量变为2.700 g,碱石灰增重0.540 g。则:
①参加反应的H2的质量为:__________;
②假设红色物质为单一物质,则红色物质的化学式为_______________。
(1)C (2)①0.060 g(或0.0600 g) ②Cu4O(或Cu2O·2Cu)
解析:
(1) H2 + CuO![]() Cu + H2O
Cu + H2O
22.4 L 79.5 g
V反应(H2) 3.180 g
V反应(H2)= ![]() =0.896 L=896 mL
=0.896 L=896 mL
由于通过玻璃管的H2,不可能全部参加反应,故所需H2体积应大于896 mL。
(2)①参加反应的H2质量为生成的水中的氢元素质量:
0.540 g-(3.180 g-2.700 g)=0.060 g(或0.540 g×![]() =0.0600 g)
=0.0600 g)
②n(CuO)= ![]() =0.0400 mol
=0.0400 mol
反应后固体中:
n(Cu)=0.0400 mol
n(O)=0.0400 mol-![]() =0.0100 mol
=0.0100 mol
[或n(O)=0.0400 mol-![]() =0.0100 mol]
=0.0100 mol]
n(Cu)∶n(O)=4∶1
红色物质化学式为:Cu4O(或Cu2O·2Cu)

 同步轻松练习系列答案
同步轻松练习系列答案
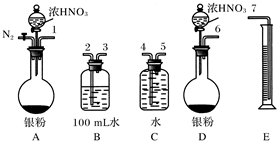

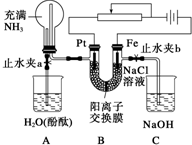 某课外活动小组设计了如图所示的装置,调节滑动变阻器,控制电流强度适中的情况下用其进行缓慢电解NaCl溶液及相关实验(此时,打开止水夹a,关闭止水夹b).由于粗心,实验并未达到预期目的,但也看到了令人很高兴的现象(阳离子交换膜只允许阳离子和水通过).
某课外活动小组设计了如图所示的装置,调节滑动变阻器,控制电流强度适中的情况下用其进行缓慢电解NaCl溶液及相关实验(此时,打开止水夹a,关闭止水夹b).由于粗心,实验并未达到预期目的,但也看到了令人很高兴的现象(阳离子交换膜只允许阳离子和水通过).