题目内容
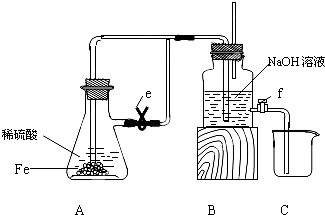
 某课外活动小组设计了如图所示的装置,调节滑动变阻器,控制电流强度适中的情况下用其进行缓慢电解NaCl溶液及相关实验(此时,打开止水夹a,关闭止水夹b).由于粗心,实验并未达到预期目的,但也看到了令人很高兴的现象(阳离子交换膜只允许阳离子和水通过).
某课外活动小组设计了如图所示的装置,调节滑动变阻器,控制电流强度适中的情况下用其进行缓慢电解NaCl溶液及相关实验(此时,打开止水夹a,关闭止水夹b).由于粗心,实验并未达到预期目的,但也看到了令人很高兴的现象(阳离子交换膜只允许阳离子和水通过).请帮助他们分析并回答下列问题:
(1)写出B装置中的电极反应:
阴极:
2H2O+2e-═H2↑+2OH-(或2H++2e-═H2↑)
2H2O+2e-═H2↑+2OH-(或2H++2e-═H2↑)
;阳极:
Fe-2e-═Fe2+
Fe-2e-═Fe2+
.(2)观察到A装置中的现象是:
①
A烧杯中的水倒吸并产生红色喷泉
A烧杯中的水倒吸并产生红色喷泉
;②
烧瓶中液面上升到高于左侧导管一定程度后又逐渐下落至与导管相平
烧瓶中液面上升到高于左侧导管一定程度后又逐渐下落至与导管相平
;③
最后A烧杯溶液呈红色,导管有气泡溢出
最后A烧杯溶液呈红色,导管有气泡溢出
.(3)当观察到A装置中的现象后,他们关闭止水夹a,打开止水夹b.再观察C装置,若无现象,请说明理由;若有现象,请写出有关反应的化学方程式(是离子反应的写离子方程式):
Fe2++2OH-═Fe(OH)2↓,4Fe(OH)2+2H2O+O2═4Fe(OH)3或写成总反应式:4Fe2++8OH-+2H2O+O2═4Fe(OH)3↓
Fe2++2OH-═Fe(OH)2↓,4Fe(OH)2+2H2O+O2═4Fe(OH)3或写成总反应式:4Fe2++8OH-+2H2O+O2═4Fe(OH)3↓
.(4)若想达到电解NaCl溶液的目的,应如何改进装置,请提出你的意见:
把Fe电极换成C、Pt等惰性电极或将装置中两电极换位置等
把Fe电极换成C、Pt等惰性电极或将装置中两电极换位置等
.分析:(1)电解氯化钠时,在电解池的阳极是活泼电极铁本身失去电子发生氧化反应,即阴极上是电解质中的阳离子发生得电子的还原反应;
(2)装置A是引发喷泉实验的装置,烧瓶内外存在压强差时就会产生喷泉,根据大气压强原理确定喷泉实验结束时的液面高低变化情况,根据溶液的酸碱性确定溶液颜色的变化情况;
(3)氢氧化钠可以和含有亚铁离子的盐发生反应生成氢氧化亚铁,氢氧化亚铁易被氧化为氢氧化铁红褐色沉淀;
(4)在电解饱和食盐水时,要实现电解氯化钠溶液的目的,应该选择惰性电极进行电解.
(2)装置A是引发喷泉实验的装置,烧瓶内外存在压强差时就会产生喷泉,根据大气压强原理确定喷泉实验结束时的液面高低变化情况,根据溶液的酸碱性确定溶液颜色的变化情况;
(3)氢氧化钠可以和含有亚铁离子的盐发生反应生成氢氧化亚铁,氢氧化亚铁易被氧化为氢氧化铁红褐色沉淀;
(4)在电解饱和食盐水时,要实现电解氯化钠溶液的目的,应该选择惰性电极进行电解.
解答:解:(1)在电解池的阳极是活泼电极本身失去电子发生氧化反应,Fe-2e-═Fe2+,阴极上是电解质中的阳离子氢离子发生得电子的还原反应,即2H2O+2e-═H2↑+2OH-(或2H++2e-═H2↑),故答案为:2H2O+2e-═H2↑+2OH-(或2H++2e-═H2↑);Fe-2e-═Fe2+;
(2)在电解池中,因为在阴极铂电极上产生了氢气,所以导致A烧杯中气压增大,氨气和水接触后,因氨气极易溶于水导致水倒吸并产生红色喷泉,当烧瓶中液面上升到高于左侧导管一定程度后又逐渐下落至与导管相平时,烧瓶内外压强相等,喷泉现象结束,由于氨水显碱性,所以最后A烧杯溶液呈红色,并且在导管有气泡氢气溢出,故答案为:A烧杯中的水倒吸并产生红色喷泉;烧瓶中液面上升到高于左侧导管一定程度后又逐渐下落至与导管相平;最后A烧杯溶液呈红色,导管有气泡溢出;
(3)在A装置中的喷泉实验后,关闭止水夹a,打开止水夹b,C装置中,含有亚铁离子的盐和其中的氢氧化钠发生反应生成氢氧化亚铁,氢氧化亚铁易被氧化为氢氧化铁红褐色沉淀,即Fe2++2OH-═Fe(OH)2↓,4Fe(OH)2+2H2O+O2═4Fe(OH)3或写成总反应式:4Fe2++8OH-+2H2O+O2═4Fe(OH)3↓,
故答案为:Fe2++2OH-═Fe(OH)2↓,4Fe(OH)2+2H2O+O2═4Fe(OH)3或写成总反应式:4Fe2++8OH-+2H2O+O2═4Fe(OH)3↓;
(4)在电解饱和食盐水时,要实现电解氯化钠溶液的目的,应该选择惰性电极进行电解,可以把Fe电极换成C、Pt等惰性电极或将装置中两电极换位置等,
故答案为:把Fe电极换成C、Pt等惰性电极或将装置中两电极换位置等.
(2)在电解池中,因为在阴极铂电极上产生了氢气,所以导致A烧杯中气压增大,氨气和水接触后,因氨气极易溶于水导致水倒吸并产生红色喷泉,当烧瓶中液面上升到高于左侧导管一定程度后又逐渐下落至与导管相平时,烧瓶内外压强相等,喷泉现象结束,由于氨水显碱性,所以最后A烧杯溶液呈红色,并且在导管有气泡氢气溢出,故答案为:A烧杯中的水倒吸并产生红色喷泉;烧瓶中液面上升到高于左侧导管一定程度后又逐渐下落至与导管相平;最后A烧杯溶液呈红色,导管有气泡溢出;
(3)在A装置中的喷泉实验后,关闭止水夹a,打开止水夹b,C装置中,含有亚铁离子的盐和其中的氢氧化钠发生反应生成氢氧化亚铁,氢氧化亚铁易被氧化为氢氧化铁红褐色沉淀,即Fe2++2OH-═Fe(OH)2↓,4Fe(OH)2+2H2O+O2═4Fe(OH)3或写成总反应式:4Fe2++8OH-+2H2O+O2═4Fe(OH)3↓,
故答案为:Fe2++2OH-═Fe(OH)2↓,4Fe(OH)2+2H2O+O2═4Fe(OH)3或写成总反应式:4Fe2++8OH-+2H2O+O2═4Fe(OH)3↓;
(4)在电解饱和食盐水时,要实现电解氯化钠溶液的目的,应该选择惰性电极进行电解,可以把Fe电极换成C、Pt等惰性电极或将装置中两电极换位置等,
故答案为:把Fe电极换成C、Pt等惰性电极或将装置中两电极换位置等.
点评:本题目是电解池的工作原理和喷泉实验相结合的一道综合知识题目,要求学生具有分析和解决问题的能力,难度较大.

练习册系列答案
相关题目