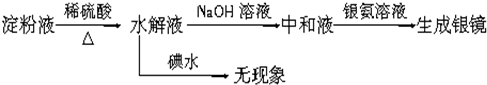
题目内容
某课外活动小组设计了如图所示的实验装置进行实验,回答下列问题: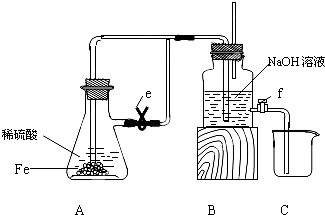
(1)开始实验时夹子e是打开的,锥形瓶A中发生反应的离子方程式为:
(2)数分钟后夹上夹子e,则试剂瓶B中可以观察到的现象是
(3)如果开启活塞f放掉约
| 2 | 3 |
分析:(1)铁和稀硫酸之间反应生成硫酸亚铁和氢气,产生气体会沿着e处导管进入B中;
(2)A中气压增加,会将生成的硫酸亚铁以及剩余的硫酸压入B中和氢氧化钠混合反应;
(3)氢氧化亚铁不稳定,容易被氧气氧化为氢氧化铁.
(2)A中气压增加,会将生成的硫酸亚铁以及剩余的硫酸压入B中和氢氧化钠混合反应;
(3)氢氧化亚铁不稳定,容易被氧气氧化为氢氧化铁.
解答:解:(1)铁和稀硫酸之间反应生成硫酸亚铁和氢气,Fe+2H+=Fe2++H2↑,夹子e是打开的,产生气体会沿着e处导管进入B中,故答案为:Fe+2H+=Fe2++H2↑;导管口有气泡冒出;
(2)A中气压增加,会将生成的硫酸亚铁以及剩余的硫酸压入B中和氢氧化钠混合反应:OH-+H+=H2O,Fe2++2OH-=Fe(OH)2,立即产生白色沉淀,
故答案为:A中溶液进入B中,立即产生白色沉淀;OH-+H+=H2O、Fe2++2OH-=Fe(OH)2.
(3)氢氧化亚铁不稳定,容易被氧气氧化为氢氧化铁,4Fe(OH)2+O2+2H2O=4Fe(OH)3,看到沉淀逐渐变为灰绿色,最后变为红褐色,
故答案为:沉淀逐渐变为灰绿色,最后变为红褐色;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(2)A中气压增加,会将生成的硫酸亚铁以及剩余的硫酸压入B中和氢氧化钠混合反应:OH-+H+=H2O,Fe2++2OH-=Fe(OH)2,立即产生白色沉淀,
故答案为:A中溶液进入B中,立即产生白色沉淀;OH-+H+=H2O、Fe2++2OH-=Fe(OH)2.
(3)氢氧化亚铁不稳定,容易被氧气氧化为氢氧化铁,4Fe(OH)2+O2+2H2O=4Fe(OH)3,看到沉淀逐渐变为灰绿色,最后变为红褐色,
故答案为:沉淀逐渐变为灰绿色,最后变为红褐色;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评:本题考查了氢氧化亚铁的制备,氢氧化亚铁不稳定,易被空气氧化生成氢氧化铁而变质,为制取氢氧化亚铁,需要将空气隔绝,只要不存在氧气就能制得较纯净的氢氧化亚铁,题目难度不大.

练习册系列答案
相关题目


 某课外活动小组设计了如图所示的装置,调节滑动变阻器,控制电流强度适中的情况下用其进行缓慢电解NaCl溶液及相关实验(此时,打开止水夹a,关闭止水夹b).由于粗心,实验并未达到预期目的,但也看到了令人很高兴的现象(阳离子交换膜只允许阳离子和水通过).
某课外活动小组设计了如图所示的装置,调节滑动变阻器,控制电流强度适中的情况下用其进行缓慢电解NaCl溶液及相关实验(此时,打开止水夹a,关闭止水夹b).由于粗心,实验并未达到预期目的,但也看到了令人很高兴的现象(阳离子交换膜只允许阳离子和水通过).