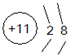��Ŀ����
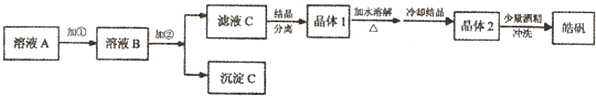
������֪��Ŀǰ�������ʼ��ѹ㷺����ʳƷ���ʡ���ʳҩ�ĵķ��棬��ù��������������Ӧ���������������ʣ���ȫ���հ�װ�ڵ��������Ӷ���װ�ڵ���Ʒ�������������á�����������ɺ���ɫʱ������ʧЧ�����±���һ���������������ʼ����䷽��
| ��Ҫԭ�� | ���� |
| ��̼4%�������� ��ʯ�� ʳ�� �ƾ� | 80% 20% 4g ���� |
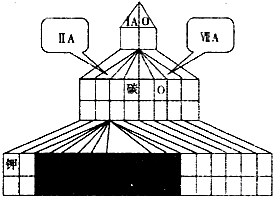
���з�Ӧʽ��������ԭ���ص��ǣ� ��
A. Fe-2e-=Fe2+ B. C+O2=CO2
C.4Fe(OH)2+O2+2H2O=4Fe(OH)3 D. 2Fe(OH)3=Fe2O3?3H2O
B

��ϰ��ϵ�д�
�����Ŀ
ijѧϰС����ͨ����ӦNa2S2O3+H2SO4�TNa2SO4+S��+SO2��+H2O�о���Ӧ���ʵ�Ӱ�����غ�Na2S2O3��������Ȥ��������֪Na2S2O3����Ϊ��������ƣ��׳ƺ��������Կ�������һ��Sԭ��ȡ����Na2SO4�е�һ��Oԭ�Ӷ��γɣ���ʵ��С���������ѧϰ��˼��Ԥ����Na2S2O3��ijЩ���ʣ���ͨ��ʵ��̽����֤�Լ���Ԥ�⣮
��������衿
��1������ѧ����ΪNa2S2O3��N2SO4�ṹ���ƣ���ѧ����Ҳ���ƣ��������ʱNa2S2O3��Һ��pH 7�����������=����������
��2������ѧ����SԪ�ػ��ϼ��Ʋ�Na2S2O3��SO2�������ƣ������н�ǿ�� ��
��ʵ��̽����
ȡ����Na2S2O3���壬����ˮ���Ƴ�Na2S2O3��Һ����������̽������д���пո�
��ʵ����ۡ�
��6��̽���٣� ��
��7��̽���ڣ� ��
���������ۡ�
��8����ͬѧ��̽���ڡ���Ӧ�����Һ�еμ���������Һ���۲쵽�а�ɫ�������������ݴ���Ϊ��ˮ�ɽ�Na2S2O3����������Ϊ�÷����Ƿ���ȷ��˵������ ��
��9������������ƶ���ʵ�鷽����֤��Na2S2O3����ˮ��������ķ����� ��
��������衿
��1������ѧ����ΪNa2S2O3��N2SO4�ṹ���ƣ���ѧ����Ҳ���ƣ��������ʱNa2S2O3��Һ��pH
��2������ѧ����SԪ�ػ��ϼ��Ʋ�Na2S2O3��SO2�������ƣ������н�ǿ��
��ʵ��̽����
ȡ����Na2S2O3���壬����ˮ���Ƴ�Na2S2O3��Һ����������̽������д���пո�
| ʵ����� | ʵ������ | ������ͣ������ӷ���ʽ��ʾ�� | |
| ̽���� | ��3�� |
��ҺpH=8 | ��4�� |
| ̽���� | ��������ˮ��pH��2���еμ�����Na2S2O3��Һ | ��ˮ��ɫ��dz | ��5�� |
��6��̽���٣�
��7��̽���ڣ�
���������ۡ�
��8����ͬѧ��̽���ڡ���Ӧ�����Һ�еμ���������Һ���۲쵽�а�ɫ�������������ݴ���Ϊ��ˮ�ɽ�Na2S2O3����������Ϊ�÷����Ƿ���ȷ��˵������
��9������������ƶ���ʵ�鷽����֤��Na2S2O3����ˮ��������ķ�����