题目内容
2.纯碱样品中常混有NaCl,通常采用沉淀法测定该样品中Na2CO3的质量分数.(1)需要向样品溶液中加入足量的CaCl2作为沉淀剂(填化学式)
(2)反应的离子方程式为Ca2++CO32-=CaCO3↓
(3)需要测量的物理量有样品的质量和生成沉淀的质量
(4)生成的沉淀需要经过过滤、洗涤、干燥,如何检验上述反应生成的沉淀是否洗净取最后一次洗涤液,加入硝酸酸化的硝酸银溶液,若无白色沉淀生成,则沉淀洗净.
分析 纯碱样品中常混有NaCl,用沉淀法测定该样品中Na2CO3的质量分数,可以将样品溶于水得溶液,在溶液中加入氯化钙得碳酸钙沉淀,生成的沉淀需要经过过滤、洗涤、干燥,根据生成沉淀的质量可计算出样品中碳酸钠的质量分数,据此答题.
解答 解:纯碱样品中常混有NaCl,用沉淀法测定该样品中Na2CO3的质量分数,可以将样品溶于水得溶液,在溶液中加入氯化钙溶液得碳酸钙沉淀,生成的沉淀需要经过过滤、洗涤、干燥,根据生成沉淀的质量结合样品的质量可计算出样品中碳酸钠的质量分数,
(1)根据上面的分析可知,需要向样品溶液中加入足量的CaCl2作为沉淀剂,故答案为:CaCl2;
(2)含有碳酸钠的样品溶液中加入氯化钙溶液得碳酸钙沉淀,反应的离子方程式为Ca2++CO32-=CaCO3↓,故答案为:Ca2++CO32-=CaCO3↓;
(3)根据上面的分析可知,需要测量的物理量有样品的质量和生成沉淀的质量,故答案为:样品的质量和生成沉淀的质量;
(4)生成的沉淀表面有氯离子杂质,所以检验上述反应生成的沉淀是否洗净的方法是取最后一次洗涤液,加入硝酸酸化的硝酸银溶液,若无白色沉淀生成,则沉淀洗净,
故答案为:取最后一次洗涤液,加入硝酸酸化的硝酸银溶液,若无白色沉淀生成,则沉淀洗净.
点评 本题以测定样品中Na2CO3的质量分数为背景,考查了物质的分离、化学实验基本操作、实验结果的处理等知识,难度中等.

练习册系列答案
相关题目
12.下列物质不能用于干燥SO2气体的是( )
| A. | 浓硫酸 | B. | 碱石灰 | C. | 无水氯化钙 | D. | 五氧化二磷 |
17.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1的Na2CO3溶液:K+、Ba2+、NO${\;}_{3}^{-}$、Cl- | |
| B. | 0.1 mol•L-1FeCl3溶液:K+、NH${\;}_{4}^{+}$、I-、OH- | |
| C. | pH=1的溶液:S2-、NH4+、Cl-、Na+ | |
| D. | 能使酚酞变红的溶液中:K+、Na+、SO${\;}_{4}^{2-}$、CH3COO- |
14.已知草酸镍晶体(NiC2O4•2H2O)难溶于水,工业上从废镍催化剂(成分主要为Ni,含有一定量的Al2O3、Fe、SiO2、CaO等)制备草酸镍晶体的流程如图所示:

已知:①相关金属离子生成氢氧化物沉淀的pH如表:
②Ksp(CaF2)=1.46×10-10
③当某物质浓度小于1.0×10-5mol•L-1时,视为完全沉淀.
(1)请写出一种能提高酸浸速率的措施把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等.
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)pH的调控范围为5.0≤pH<6.8.
(4)写出“沉镍”时反应的离子方程式Ni2++C2O42-+2H2O=NiC2O4•2H2O,当Ca2+沉淀完全时,溶液中c(F-)>$\sqrt{\frac{1.46×10{\;}^{-10}}{10{\;}^{-5}}}$mol•L-1(写出计算式即可).

已知:①相关金属离子生成氢氧化物沉淀的pH如表:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
| 完全沉淀的PH | 3.2 | 8.8 | 5.0 | 9.5 |
③当某物质浓度小于1.0×10-5mol•L-1时,视为完全沉淀.
(1)请写出一种能提高酸浸速率的措施把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等.
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)pH的调控范围为5.0≤pH<6.8.
(4)写出“沉镍”时反应的离子方程式Ni2++C2O42-+2H2O=NiC2O4•2H2O,当Ca2+沉淀完全时,溶液中c(F-)>$\sqrt{\frac{1.46×10{\;}^{-10}}{10{\;}^{-5}}}$mol•L-1(写出计算式即可).
12.下列关于新制氯水及久置氯水的说法,不正确的是( )
| A. | 新制的氯水呈浅黄绿色,久置的氯水无色 | |
| B. | 新制的氯水漂白作用强,而久置的氯水漂白作用很弱 | |
| C. | 新制的氯水所含成分多,而久置的氯水所含成分少 | |
| D. | 新制的氯水中无氯离子,而久置的氯水中则含氯离子 |

 实验是化学研究的一种重要手段,现有如图所示A~G七种仪器,请根据要求填空.
实验是化学研究的一种重要手段,现有如图所示A~G七种仪器,请根据要求填空.
 和
和 E、CH3CH2CH2CH3和
E、CH3CH2CH2CH3和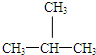
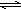 HCO3-+OH-
HCO3-+OH- 的系统命名为:3-甲基-4-乙基-庚烷
的系统命名为:3-甲基-4-乙基-庚烷 .
.