题目内容
14.(1)Na、Cu、Si、H、C、N六种元素,其对应单质的熔点按照A、B、C、D、E、F的顺序依次升高,其中C、D均是热和电的良导体.①请写出B单质对应元素原子的电子排布式1s22s22p3.
②单质A、F对应的元素以原子个数比1:1形成的气态化合物分子中含3个σ键和2个π键.
③A与B对应的元素形成的10电子分子X的空间构型为三角锥形;将X溶于水后的溶液滴入到CuSO4溶液中至过量,得到络离子的化学式为[Cu(NH3)4]2+,其中X与Cu2+之间以配位键结合.
④如图是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:
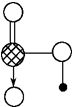
a.HNO3是极性分子,易溶于极性的水中
b.HNO3分子中的-OH易与水分子之间形成氢键
(2)碳是形成化合物最多的元素,其单质与化合物广布于自然界.
①与碳同周期的非金属元素N的第一电离能大于O的第一电离能,原因是N原子2p轨道半充满,能量低;
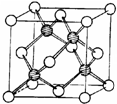
②冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立方体内)类似.每个冰晶胞平均占有8个水分子,冰晶胞与金刚石晶胞微粒排列方式相同的原因是水中的O和金刚石中的C都是sp3杂化,且水分子间的氢键具有方向性,每个水分子可与相邻的4个水分子形成氢键.
 ?
?(3)在NaCl晶体中,阴、阳离子具有或近似具有球型对称结构,它们可以被看作刚性圆球,并彼此“相切”.如图为NaCl的晶胞结构图及晶胞的剖面图:
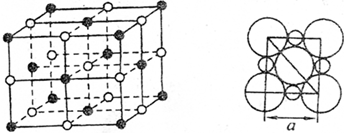
若a=5.6×10-8cm,则该晶体的密度为2.2g/cm3(精确到小数点后1位)
分析 (1)Na、Cu、Si、H、C、N六种元素,其对应单质的熔点按照A、B、C、D、E、F的顺序依次升高,其中C、D均是热和电的良导体,则C、D为金属,根据熔点比较可知,C为Na,D为Cu,其它四种单质根据熔点高低的顺序可知A为H2,B为N2,E为Si,F为C,A与B对应的元素形成的10电子分子X为NH3,图1是上述六种元素中的一种元素形成的含氧酸的结构,则该酸为HNO3;
(2)①原子轨道中的电子处于全满、半满、全空时最稳定;
②利用均摊法确定每个冰晶胞含有的水分子个数,根据氧原子和碳原子的杂化方式分析;
(3)由Na、Cl两元素形成的化合物为NaCl,晶胞中Na+离子数目=1+12×$\frac{1}{4}$=4,Cl-离子数目=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,故晶胞质量=$\frac{4×58.5}{6.02×10{\;}^{23}}$g,晶胞体积=(5.6×10-8cm)3,据此计算晶胞的密度;
解答 解:(1)Na、Cu、Si、H、C、N六种元素,其对应单质的熔点按照A、B、C、D、E、F的顺序依次升高,其中C、D均是热和电的良导体,则C、D为金属,根据熔点比较可知,C为Na,D为Cu,其它四种单质根据熔点高低的顺序可知A为H2,B为N2,E为Si,F为C,A与B对应的元素形成的10电子分子X为NH3,图1是上述六种元素中的一种元素形成的含氧酸的结构,则该酸为HNO3,
①B为N2,B单质对应元素原子的电子排布式为1s22s22p3,
故答案为:1s22s22p3;
②A为H2,F为C,单质A、F对应的元素以原子个数比1:1形成的气态化合物为C2H2,C2H2分子中含3个σ键和2个π键,
故答案为:3;2;
③X为NH3,NH3中氮原子的价层电子对数为$\frac{5+3}{2}$=4,有一对孤电子对,所以NH3空间构型为三角锥形,将NH3溶于水后的溶液滴入到CuSO4溶液中至过量,得到络离子的化学式为[Cu (NH3)4]2+,其中NH3与Cu2+之间以配位键结合,
故答案为:三角锥形;[Cu (NH3)4]2+;配位;
④图1中的含氧酸为HNO3,HNO3易溶于水的原因a.HNO3是极性分子,易溶于极性的水中;b.HNO3分子中的-OH易与水分子之间形成氢键,
故答案为:HNO3是极性分子,易溶于极性的水中;HNO3分子中的-OH易与水分子之间形成氢键;
(2)①N原子的核外电子排布式为:1s22s22p3,O原子核外电子排布式为1s22s22p4,2p轨道半充满的原子能量低,较稳定,所以与碳同周期的非金属元素N的第一电离能大于O的第一电离能;
故答案为:N原子2p轨道半充满,能量低;
②每个冰晶胞平均占有分子个数=4+$\frac{1}{8}$×8+$\frac{1}{2}$×6=8,H2O的氧原子中含有2个σ键和2个孤电子对,金刚石中每个碳原子含有4个σ键且没有孤电子对,所以水中的O和金刚石中的C都是sp3杂化,且水分子间的氢键具有方向性,每个水分子中一个氧原子可以和另外2个水分子形成2个原子,2个氢原子可以和另外2个水分子形成氢键,所以每个水分子可与相邻的4个水分子形成氢键,导致冰晶胞与金刚石晶胞微粒排列方式相似,
故答案为:8;水中的O和金刚石中的C都是sp3杂化,氢键具有方向性,每个水分子与相邻的4个水分子形成氢键;
(3)由Na、Cl两元素形成的化合物为NaCl,晶胞中Na+离子数目=1+12×$\frac{1}{4}$=4,Cl-离子数目=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,故晶胞质量=$\frac{4×58.5}{6.02×10{\;}^{23}}$g,晶胞体积=(5.6×10-8cm)3,则该晶体的密度ρ=$\frac{4×58.5}{6.02×10{\;}^{23}}$g÷(5.6×10-8cm)3=2.2 g•cm-3;
故答案为:2.2;
点评 本题考查较为综合,涉及电子排布、化学键、分子结构与性质、配合物、第一电离能、晶胞计算等,推断元素是解题关键,注意利用均摊法进行晶胞计算,侧重考查了学生对知识的综合运用和掌握,难度中等.

| A. | 糖中混有少量食盐 | B. | 氯化钠中混有少量泥沙 | ||
| C. | 食盐中混有少量硝酸钾 | D. | 水中混有酒精 |
| A. | 乙烯和2-丁烯 | B. | 苯和乙炔 | ||
| C. | 1-氯丙烷和2-氯丙烷 | D. | 异丁烷和正戊烷 |
| A. | 醋酸溶液 | B. | 豆浆 | C. | 氢氧化铁沉淀 | D. | 蔗糖 |
| A. | 在c(H+)=1.0×10-13 mol•L-1的溶液中:Na+、S2-、AlO2-、SO32- | |
| B. | pH<7的溶液中:SO42-、CO32-、Na+、K+ | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| D. | 在pH=1的溶液中:NH4+、K+、ClO-、Cl- |
| A. |  石油分馏 | B. |  灼烧干海带 | ||
| C. |  用CCl4萃取碘水中的碘 | D. |  治炼金属铁 |
| A. | 原子最外层电子数为2的元素一定处于周期表ⅡA族 | |
| B. | 主族元素X、Y能形成XY2型化合物,则X与Y的原子序数之差可能为2或5 | |
| C. | 氯化氢的沸点比氟化氢的沸点高 | |
| D. | 同主族元素形成的氧化物的晶体类型均相同 |
| A. | 分解复分解 | B. | 氧化化合 | C. | 复分解中和 | D. | 置换氧化还原 |
 .
.