题目内容
2.近年来,华北地区雾霾时有发生,这与汽车尾气、工业生产排放的大量有害气体有关.下列反应中,B、C是空气质量监测的物质,其中C是红棕色气体,D是强酸(部分反应条件和产物已经略去).A$\stackrel{O_{2}}{→}$B$\stackrel{O_{2}}{→}$C$\stackrel{H_{2}O}{→}$D
(1)若A是气体单质,则A生成B的化学方程式为N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO
(2)若A为气态氢化物且水溶液呈碱性,则A的电子式为
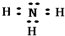 ,写出A在生产生活中的一种用途合成硝酸或氮肥
,写出A在生产生活中的一种用途合成硝酸或氮肥(3)D的浓溶液与铜反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
分析 C是红棕色气体,B与氧气反应生成C,则C为NO2,D为HNO3,
(1)若A是气体单质,则A为N2,B为NO;
(2)若A为气态氢化物且水溶液呈碱性,则A为NH3,B为NO,氨气为重要的化工原料,液氨经常作制冷剂;
(3)D的浓溶液与铜反应生成硝酸铜、二氧化氮和水.
解答 解:B、C是空气质量监测的物质,结合A$\stackrel{O_{2}}{→}$B$\stackrel{O_{2}}{→}$C$\stackrel{H_{2}O}{→}$D,C是红棕色气体,B与氧气反应生成C,则C为NO2,D为HNO3,
(1)若A是气体单质,则A为N2,B为NO,A生成B的化学方程式为N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO,
故答案为:N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO;
(2)若A为气态氢化物且水溶液呈碱性,则A为NH3,其电子式为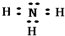 ,A在生产生活中的一种用途为合成硝酸、氮肥等或作制冷剂,
,A在生产生活中的一种用途为合成硝酸、氮肥等或作制冷剂,
故答案为: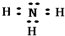 ;合成硝酸或氮肥;
;合成硝酸或氮肥;
(3)D为硝酸,浓硝酸和铜反应生成硝酸铜、二氧化氮和水,反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,
故答案为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
点评 本题考查无机物的推断,为高频考点,把握C为红棕色的气体且为氧化物可知C二氧化氮为解答的关键,侧重分析与推断能力的考查,注意含N物质的性质及相互转化的应用,题目难度不大.

练习册系列答案
相关题目
8.下列说法不正确的是( )
| A. | 苯酚的俗称:石炭酸 | |
| B. | CH3COCH3分子中的官能团名称:醚键 | |
| C. | 葡萄糖的实验式:CH2O | |
| D. | 乙炔的结构简式:CH≡CH |
9.下列说法正确的是( )
| A. | 二氧化硅既不溶于水也不溶于任何酸 | |
| B. | 二氧化碳通入饱和氯化钙溶液中能生成白色沉淀 | |
| C. | 二氧化碳通入硅酸钠溶液中可以得到硅酸 | |
| D. | 二氧化硅是制造玻璃的主要原料,它不能与氢氧化钠溶液反应 |
6.下列叙述正确的是( )
| A. | 摩尔是表示物质的量的多少的基本物理量 | |
| B. | 0.012kg12C中含有约6.02×1023个碳原子 | |
| C. | 氢氧化钠的摩尔质量是40g | |
| D. | 2mol水的摩尔质量是1mol水的摩尔质量的2倍 |
7.下面的排序不正确的是( )
| A. | 含氧酸酸性强弱:HClO4>HClO3>HClO2>HClO | |
| B. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| C. | 熔点由高到低:Na>Mg>Al | |
| D. | 晶格能由大到小:NaF>NaCl>NaBr>NaI |
14.下列叙述或实验现象描述正确的是( )
| A. | 将铜与浓硫酸共热,产生使石蕊溶液变红的气体,说明浓硫酸具有酸性 | |
| B. | 往足量铁与稀硝酸反应后的溶液中滴入KSCN溶液,溶液变为血红色 | |
| C. | 往FeSO4溶液中通入NO2气体,溶液始终无明显现象 | |
| D. | 往BaCl2溶液中通入SO2气体,无沉淀产生,再通NH3,产生白色沉淀 |
12.以下说法正确的是( )
| A. | C60与金刚石一样属于原子晶体 | |
| B. | 由非金属元素组成的化合物一定是共价化合物 | |
| C. | 分子晶体中必含化学键 | |
| D. | 干冰升华时,分子内的共价键未发生断裂 |