题目内容
a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且碱性b>a,c和d的气态氢化物的还原性d>c,五种元素的原子,得失电子后所形成的简单离子中,e的还原性性最强,则它们的原子序数由小到大的顺序是( )
| A、b、a、e、d、c |
| B、e、d、a、b、c |
| C、a、b、d、c、e |
| D、c、d、e、a、b |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:根据同周期元素从左到右金属性逐渐减弱,非金属性逐渐增强可知,a、b,c、d的原子序数关系,根据离子还原性的变化规律可知e与a、b、c、d的原子序数关系.
解答:
解:a和b的最高价氧化物对应水化物呈碱性,则a、b为金属,且失电子能力b>a(其最高价氧化物对应水化物的碱性b>a);c和d的气态氢化物的还原性d>c,即c、d为非金属,且得电子能力d<c.根据同周期元素从左到右失电子能力逐渐减弱,得电子能力逐渐增强的规律,将a、b、c、d四种元素大致排序为: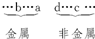 因为五种元素的原子得失电子后所形成的简单离子中,e的还原性性最强,则e应为非金属元素,同周期离子还原性从左到右减弱,故e原子序数介于a和d之间,
因为五种元素的原子得失电子后所形成的简单离子中,e的还原性性最强,则e应为非金属元素,同周期离子还原性从左到右减弱,故e原子序数介于a和d之间,
故选A.
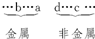 因为五种元素的原子得失电子后所形成的简单离子中,e的还原性性最强,则e应为非金属元素,同周期离子还原性从左到右减弱,故e原子序数介于a和d之间,
因为五种元素的原子得失电子后所形成的简单离子中,e的还原性性最强,则e应为非金属元素,同周期离子还原性从左到右减弱,故e原子序数介于a和d之间,故选A.
点评:本题考查原子结构与元素周期律的关系,题目难度中等,注意同周期元素的性质的递变规律,注意离子还原性的比较方法.

练习册系列答案
相关题目
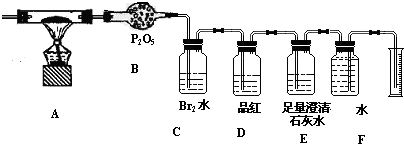
根据下列化学实验示意图,能得出正确结论的是( )
A、 配置一定浓度的烧碱溶液 |
B、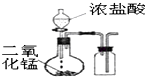 制取并收集Cl2 |
C、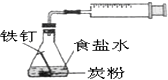 铁的析氢腐蚀 |
D、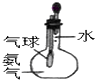 验证氨气易溶于水 |