题目内容
20.下列各组混合物,可以用分液漏斗分离的是( )| A. | 水和酒精 | B. | 四氯化碳和水 | C. | 溴和溴苯 | D. | 汽油和煤油 |
分析 可以用分液漏斗分离,则选项中的物质不相溶,出现分层,以此来解答.
解答 解:A.水和酒精互溶,不分层,故A不选;
B.四氯化碳和水分层,可以用分液漏斗分离,故B选;
C.溴和溴苯互溶,不分层,故C不选;
D.汽油和煤油互溶,不分层,故D不选;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离提纯方法为解答的关键,侧重分析与应用能力的考查,注意有机物的溶解性,题目难度不大.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
11.以下化学用语正确的是( )
| A. | 苯的最简式:C6H6 | B. | 甲醛的结构式: | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 乙醇的分子式:CH3CH2OH |
5.下列说法正确的是( )
| A. | 化合反应均是放热反应 | B. | 中和反应都是放热反应 | ||
| C. | 吸热反应只吸收外界能量 | D. | 氧化还原反应均是放热反应 |
12.为提纯下列物质(括号内为杂质)选用的试剂和分离方法都正确的是( )
| 物质 | 试剂 | 分离方法 | |
| ① | 溴苯(溴) | 氢氧化钠溶液 | 分液 |
| ② | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
| ③ | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| ④ | Cl2(HCl) | 饱和NaCl溶液 | 洗气 |
| A. | ①③ | B. | ①④ | C. | 只有 ④ | D. | ③④ |
9.下列说法正确是( )
| A. | 4.6g有机物C2H6O的分子结构中含有的C-H键数目一定为0.5Na | |||||||||||
| B. | 用惰性电极电解足量氯化钠溶液,当阴极生成气体质量为2g时,溶液中转移电子数为2Na | |||||||||||
| C. | 一定温度下,若用Kw表示水的离子积,Kb表示一水合氨的电离常数,则该温度下水解平衡常数K=$\frac{{K}_{W}}{{K}_{b}}$ | |||||||||||
| D. | 已知如表所示数据:
|
19.下列实验中均需要的仪器是( )
①蒸发 ②PH试纸的使用 ③过滤.
①蒸发 ②PH试纸的使用 ③过滤.
| A. | 试管 | B. | 胶头滴管 | C. | 玻璃棒 | D. | 漏斗 |
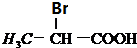 ,请回答下列问题.
,请回答下列问题. .
.