题目内容
15.含硫化合物是自然界中最为重要的自然资源之一,在生产生活中应用非常广泛.(1)燃煤烟气的脱硫(除SO2)技术和脱硝(除NOx)技术是环境科学研究的热点.以下是用硫和氮的氧化物之间的相互转化联合进行的脱硫和脱硝技术反应的热化学方程式.
NO2(g)+SO2(g)+H2O(l)=H2SO4(l)+NO(g)△H=a kJ•mol-1
2NO(g)+O2(g)=2NO2(g)△H=b kJ•mol-1
①反应2SO2(g)+O2(g)+2H2O(l)=2H2SO4(l)的△H=2a+bkJ•mol-1(用含a、b的代数式表示).
②将SO2通入硫酸铁溶液也能发生类似的反应.请写出该反应的离子方程式SO2+2Fe3++2H2O=SO42-+2Fe2++4H+.
(2)MnSO4是最重要的基础锰盐.工业上,生产MnSO4的方法有多种.
①一种较为环保的方法是:利用纤维素水解产物还原软锰矿的方法生产MnSO4,其反应方程式如下:(C6H10O5)n+n H2SO4→n(C6H11O5)HSO4
n(C6H11O5)HSO4+n H2O→n C6H12O6+n H2SO4
C6H12O6+12H2SO4+12MnO2→12MnSO4+6CO2↑+18H2O
从理论上讲,每生产1吨MnSO4需要的纤维素的质量为0.09t.
②软锰矿中都含有一定量的砷的化合物,如果不除砷很难达到饲料级的生产标准.工业上常用氧化剂来除去其中的砷.可以除去砷的氧化剂有:ClO-、KMnO4、(NH4)2S2O8、O3、H2O2等,但在实际生产中,选用的氧化剂是软锰矿,可能的原因是降低成本,不增加新的杂质.
③在生产MnSO4的浸出渣中常会产生一些硫磺,可以利用四氯乙烯来回收硫磺,回收硫磺过程中受外界影响较大的因素主要有:萃取温度、液固比等.下图1是上述3种因素对萃取硫磺质量影响的关系图.
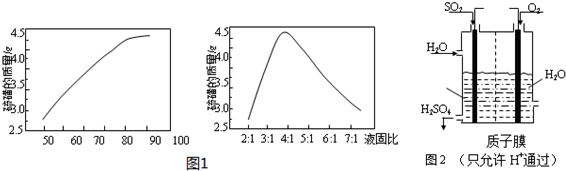
请根据以上图表信息,选择最佳的萃取温度和液固比80℃、4:1.
(3)有人设想用电化学法将SO2转化为H2SO4的原理如图2所示.
①该电解质溶液中质子的流向是从负极流向正极;(填“从正极流向负极”或“从负极流向正极”)
②写出该电池负极反应的电极反应方程式:SO2+2H2O-2e-=SO42-+4H+.
分析 (1)①已知:①NO2(g)+SO2(g)+H2O(l)=H2SO4(l)+NO(g)△H=a kJ•mol-1
②2NO(g)+O2(g)=2NO2(g)△H=b kJ•mol-1
由盖斯定律可知,方程式①×2+②可得2SO2(g)+O2(g)+2H2O(l)=2H2SO4(l),据此计算;
②铁离子具有氧化性能把二氧化硫氧化为硫酸根离子;
(2)①根据方程式中物质之间的关系计算;
②除杂质不能引入新的杂质,工业生产还有考虑成本;
③根据题中所给的图象分析;
(3)①原电池中阳离子向正极移动;
②负极上二氧化硫失电子生成硫酸根离子.
解答 解:(1)①已知:①NO2(g)+SO2(g)+H2O(l)=H2SO4(l)+NO(g)△H=a kJ•mol-1
②2NO(g)+O2(g)=2NO2(g)△H=b kJ•mol-1
由盖斯定律可知,方程式①×2+②可得2SO2(g)+O2(g)+2H2O(l)=2H2SO4(l),△H=2a+b kJ•mol-1,
故答案为:2a+b;
②铁离子具有氧化性能把二氧化硫氧化为硫酸根离子,则SO2通入硫酸铁溶液反应的离子方程式为SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;
故答案为:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;
(2)①已知:(C6H10O5)n+n H2SO4→n(C6H11O5)HSO4
n(C6H11O5)HSO4+n H2O→n C6H12O6+n H2SO4
C6H12O6+12H2SO4+12MnO2→12MnSO4+6CO2↑+18H2O
则(C6H10O5)n~~n(C6H11O5)HSO4~~n C6H12O6~~12n MnSO4
162n 1812n
xt 1t
解得x=0.09t;
故答案为:0.09t;
②除杂质不能引入新的杂质,所以不能选用ClO-、KMnO4、(NH4)2S2O8,工业生产还有考虑成本,选择软锰矿作氧化剂可以降低生成成本;
故答案为:降低成本,不增加新的杂质;
③由题中所给的图象可知,在80℃和液固比为4:1时,硫磺的萃取质量较大;
故答案为:80℃、4:1;
(3)①二氧化硫和氧气形成原电池,二氧化硫失电子为负极,氧气得电子为正极,溶液中阳离子向正极移动,所以电解质溶液中质子的流向是从负极流向正极;
故答案为:从负极流向正极;
②负极上二氧化硫失电子生成硫酸根离子,则负极电极方程式为:SO2+2H2O-2e-=SO42-+4H+;
故答案为:SO2+2H2O-2e-=SO42-+4H+.
点评 本题考查了盖斯定律的应用、氧化还原反应和离子方程式的书写、有关方程式的计算原电池原理的应用,题目涉及的知识点较多,侧重于考查学生对基础知识的应用能力和计算能力,题目难度中等,注意对有关知识的掌握以及归纳整理.

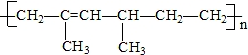
| A. | 乙烯和2-甲基-1,3-戊二烯 | B. | 2,4-二甲基-1,3-己二烯 | ||
| C. | 2,4-二甲基-2-已烯 | D. | 乙烯和2-甲基-1,3-丁二烯 |
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊不消失 | Na[Al(OH)4]溶液 |
| B | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失 | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊.再加入品红溶液,红色褪去 | Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,又变浑浊 | Ca(OH)2溶液 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 金属钠投入水中:Na+H2O═Na++OH-+H2↑ | |
| B. | 足量铁加入少量稀硝酸中:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| C. | 向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3•H2O+2H2O | |
| D. | 用银氨溶液检验乙醛中的醛基:CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+2Ag↓+H2O |
| A. | 水和酒精 | B. | 四氯化碳和水 | C. | 溴和溴苯 | D. | 汽油和煤油 |
| A. | C2H6 | B. | C2H6O | C. | C2H4O | D. | C3H6 |
| A. | 气态氢化物的稳定性强弱:HF>HCl>HBr>HI | |
| B. | 原子半径大小:Mg>S>O | |
| C. | 碱性强弱:NaOH<Mg(OH)2 | |
| D. | 金属性强弱:K>Na |
 图乙为一个金属铜的晶胞,请完成以下各题.
图乙为一个金属铜的晶胞,请完成以下各题.