题目内容
下列反应中Cl元素全部被氧化的是( )
| A、KClO3+6HCl=KCl+3Cl2↑+3H2O | ||||
B、2NaCl
| ||||
C、H2+Cl2
| ||||
| D、2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O |
考点:氧化还原反应
专题:氧化还原反应专题
分析:Cl元素全部被氧化,则Cl失去电子,Cl元素的化合价升高,以此来解答.
解答:
解:A.氯酸钾中Cl元素的化合价降低,HCl中Cl元素的化合价升高,Cl元素既被氧化又被还原,故A不选;
B.Cl元素的化合价升高,全部被氧化,故B选;
C.Cl元素的化合价降低,被还原,故C不选;
D.Cl元素的化合价既升高又降低,Cl元素既被氧化又被还原,故D不选;
故选B.
B.Cl元素的化合价升高,全部被氧化,故B选;
C.Cl元素的化合价降低,被还原,故C不选;
D.Cl元素的化合价既升高又降低,Cl元素既被氧化又被还原,故D不选;
故选B.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化解答的关键,侧重氧化反应的考查,注意从化合价角度分析,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
下列说法正确的是( )
| A、常温常压下,11.2L氮气所含的原子数为NA |
| B、常温常压下,1mol O3含有的核外电子数为4NA |
| C、18水所含的电子数目为10NA |
| D、同温同压下,相同体积的任何气体单质所含的原子数目相同 |
下列电离方程式书写错误的是( )
| A、CaCl2=Ca2++2Cl- |
| B、NaHSO4=Na++H++SO42- |
| C、HNO3=H++NO3- |
| D、KOH=K++O2-+H+ |
| E、KOH=K++O2-+H+ |
下列各组试剂(括号内的是滴加试剂)做溶液导电性实验的过程中,可以观察到灯泡由亮变暗直至熄灭,然后又逐渐变亮的是( )
| A、BaCl2溶液(稀硫酸) |
| B、氨水(醋酸溶液) |
| C、Ba(OH)2溶液[Ba(HCO3)2溶液] |
| D、Ba(OH)2溶液(NaHSO4溶液) |
下列有机物的命名正确的是( )
A、 :2,2,4三甲基戊烷 :2,2,4三甲基戊烷 |
| B、CH3CHO:甲酸 |
C、 :2乙基3丁烯 :2乙基3丁烯 |
D、 :2-羟基丁烷 :2-羟基丁烷 |
已知重铬酸钾(K2Cr2O7)是一种比高锰酸钾还要强的氧化剂,其溶液中存在如下平衡:
2CrO42-(黄色)+2H +?Cr2O72-(橙色)+H2O若要使溶液的橙色加深,下列可采用的方法是( )
2CrO42-(黄色)+2H +?Cr2O72-(橙色)+H2O若要使溶液的橙色加深,下列可采用的方法是( )
| A、加入适量烧碱固体 |
| B、加入适量稀盐酸 |
| C、加入适量稀硫酸 |
| D、加水稀释 |
下列物质既能发生消去反应,又能氧化成醛的是( )
| A、CH3CHOHCH3 |
B、 |
C、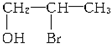 |
D、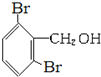 |