题目内容
已知NaOH固体中混有少量NaHCO3固体,取一定质量的这种固体混合物在密闭容器中加热到250℃左右,待充分反应后冷却至室温,将残留固体溶于水,取出![]() 该溶液,加入10g 26.95%稀硫酸恰好完全反应,并得到0.22g CO2气体.则该固体混合物中NaHCO3的质量是________,残留固体与H2SO4的反应方程式为________,生成Na2SO4质量是________.
该溶液,加入10g 26.95%稀硫酸恰好完全反应,并得到0.22g CO2气体.则该固体混合物中NaHCO3的质量是________,残留固体与H2SO4的反应方程式为________,生成Na2SO4质量是________.
答案:
解析:
提示:
解析:
|
4.2g,2NaOH+H2SO4=Na2SO4+2H2O,Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,3.9g |
提示:
|
提示:混合固体加热时发生化学反应NaOH+NaHCO3=Na2CO3+H2O,残留固体Na2CO3,可能有NaOH,其中Na2CO3+H2SO4=Na2SO4+H2O+CO2↑则NaHCO3~CO2,得出NaHCO3质量0.42g Na2SO4的质量可利用 Na2SO4——H2SO4 142 98 m 10×26.95% |

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
 实验化学
实验化学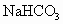 固体,取一定质量的这种固体混合物在密闭容器中加热到250℃左右,待充分反应后冷却至室温,将残留固体溶于水后取出1/10该溶液,加入10g质量分数为26.95%
固体,取一定质量的这种固体混合物在密闭容器中加热到250℃左右,待充分反应后冷却至室温,将残留固体溶于水后取出1/10该溶液,加入10g质量分数为26.95%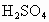 溶液恰好完全反应,并得到0.22g
溶液恰好完全反应,并得到0.22g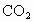 气体.求该固体混合物中NaOH的质量分数.
气体.求该固体混合物中NaOH的质量分数.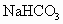 固体,取一定质量的这种固体混合物在密闭容器中加热到250℃左右,待充分反应后冷却至室温,将残留固体溶于水后取出1/10该溶液,加入10g质量分数为26.95%
固体,取一定质量的这种固体混合物在密闭容器中加热到250℃左右,待充分反应后冷却至室温,将残留固体溶于水后取出1/10该溶液,加入10g质量分数为26.95% 溶液恰好完全反应,并得到0.22g
溶液恰好完全反应,并得到0.22g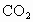 气体.求该固体混合物中NaOH的质量分数.
气体.求该固体混合物中NaOH的质量分数.