题目内容
一定量的锌粒与100mL一定浓度的硫酸充分反应后生成的气体为0.3moL,则反应消耗H2SO4的物质的量和原H2SO4的物质的量浓度肯定不正确的是( )
| A、n(H2SO4)=0.6mol c(H2SO4)>6mol/L |
| B、n(H2SO4)=0.3mol c(H2SO4)≥3mol/L |
| C、n(H2SO4)<0.3mol c(H2SO4)<3mol/L |
| D、0.3mol≤n(H2SO4)≤0.6mol 3mol/L≤c(H2SO4)≤6mol/L |
考点:化学方程式的有关计算
专题:
分析:锌与浓硫酸发生:Zn+2H2SO4═ZnSO4+SO2↑+2H2O,随着反应的进行,硫酸浓度降低,发生:Zn+H2SO4═ZnSO4+H2↑,生成气体为SO2和H2的混合物,一定量的锌粒与100mL一定浓度的硫酸充分反应后不论是否生成氢气,生成的气体为0.3moL,根据得失电子守恒,参加反应锌的物质的量为:0.3mol,硫酸锌的物质的量为0.3mol,如果只生成氢气,则反应消耗H2SO4的物质的量为0.3mol 和原H2SO4的物质的量浓度为3mol/L;如果全部生成二氧化硫,则氧化性硫酸为0.3mol,酸性硫酸也是0.3mol,随反应的进行浓硫酸变稀硫酸,所以反应消耗H2SO4的物质的量为0.6mol和原H2SO4的物质的量浓度肯定大于6mol/L,由此分析解答.
解答:
解:锌与浓硫酸发生:Zn+2H2SO4═ZnSO4+SO2↑+2H2O,随着反应的进行,硫酸浓度降低,发生:Zn+H2SO4═ZnSO4+H2↑,生成气体为SO2和H2的混合物,一定量的锌粒与100mL一定浓度的硫酸充分反应后不论是否生成氢气,生成的气体为0.3moL,根据得失电子守恒,参加反应锌的物质的量为:0.3mol,硫酸锌的物质的量为0.3mol,如果只生成氢气,则反应消耗H2SO4的物质的量为0.3mol 和原H2SO4的物质的量浓度为3mol/L;如果全部生成二氧化硫,则氧化性硫酸为0.3mol,酸性硫酸也是0.3mol,随反应的进行浓硫酸变稀硫酸,所以反应消耗H2SO4的物质的量为0.6mol和原H2SO4的物质的量浓度肯定大于6mol/L,
A、生成的气体全部是二氧化硫,反应消耗H2SO4的物质的量为0.6mol和原H2SO4的物质的量浓度肯定大于6mol/L,故A正确;
B、是稀硫酸与一定量的锌反应,酸过量,得反应消耗n(H2SO4)=0.3mol,原c(H2SO4)≥3mol/L,故B正确;
C、不管是稀硫酸还是浓硫酸反应消耗H2SO4的物质的量大于等于0.3mol,故C错误;
D、生成的气体是氢气和二氧化硫的混合气体,符合0.3mol≤反应消耗H2SO4的物质的量≤0.6mol,3mol/L≤原H2SO4的物质的量浓度≤6mol/L,故D正确;
故选C.
A、生成的气体全部是二氧化硫,反应消耗H2SO4的物质的量为0.6mol和原H2SO4的物质的量浓度肯定大于6mol/L,故A正确;
B、是稀硫酸与一定量的锌反应,酸过量,得反应消耗n(H2SO4)=0.3mol,原c(H2SO4)≥3mol/L,故B正确;
C、不管是稀硫酸还是浓硫酸反应消耗H2SO4的物质的量大于等于0.3mol,故C错误;
D、生成的气体是氢气和二氧化硫的混合气体,符合0.3mol≤反应消耗H2SO4的物质的量≤0.6mol,3mol/L≤原H2SO4的物质的量浓度≤6mol/L,故D正确;
故选C.
点评:本题考查氧化还原反应的计算,侧重于硫酸的性质的考查,注意浓硫酸和稀硫酸性质的异同,题目难度不大.

练习册系列答案
相关题目
下列各组物质中,物质之间通过一步反应就能实现图示转化的是( )
| 物质编号 | 物质转化关系 | a | b | c | d |
| ① | 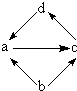 | FeCl2 | Fe | FeCl3 | CuCl2 |
| ② | Na2O | Na | Na2O2 | Mg(OH)2 | |
| ③ | NO | N2 | NO2 | NaCl | |
| ④ | Al2O3 | Al | Na[Al(OH)4] | Al(OH)3 |
| A、①②③ | B、①③④ |
| C、①④ | D、②④ |
短周期元素X、Y、Z、W、Q的原子序数依次增大,且只有一种金属元素.其中X与W处于同一主族,Z元素原子半径在短周期中最大(稀有气体除外).W、Z之间与W、Q之间原子序数之差相等,五种元素原子最外层电子数之和为21,下列说法正确的是( )
| A、Y的简单离子半径小于Z的简单离子半径 |
| B、Z最高价氧化物对应的水化物分别与X、Y最高价氧化物对应的水化物反应生成1mol水时所放出的热量相同 |
| C、Y的简单气态氢化物在一定条件下可被Q单质氧化 |
| D、Q可分别与X、Y、Z、W形成化学键类型相同的化合物 |
2013年10月,三位美国化学家因为给复杂化学体系设计了多尺度模型而荣获诺贝尔化学奖.模型由C、H、O的两种或三种原子构成,有关说法错误的是( )
| 序号 | 1 | 2 | 3 | 4 |
| 模型示意图 |  |  |  |  |
| A、模型1对应的物质的二氯代物有2种 |
| B、模型2对应的物质的官能团是羧基 |
| C、模型2对应的物质与模型3对应的物质能发生酯化反应 |
| D、模型4对应的物质可以与氯气发生加成反应 |
下列说法不正确的是( )
| A、不能用氯气消毒后的自来水配制FeCl2溶液 |
| B、过氧化钠与水的反应中水既不作氧化剂也不作还原剂 |
| C、等质量的钠投入到足量水中和将钠用铝箔包好并刺一些小孔再放人足量的水中生成氢气一样多 |
| D、铁制品要防锈而铝制品却不要防锈,这是由于铝表面易形成一层致密的氧化膜 |