题目内容
以石墨为电极材料进行电解,下列说法正确的是( )
| A、电解NaOH溶液时,溶液浓度将减小 |
| B、电解H2SO4溶液时,溶液浓度将减小 |
| C、电解Na2SO4溶液时,溶液浓度将增大 |
| D、电解NaCl溶液时,溶液浓度将增大 |
考点:电解原理
专题:电化学专题
分析:以石墨为电极电解含氧酸、强碱、氢之前金属的含氧酸盐溶液时,实质上是电解水,如果用石墨电解氢之前金属的氯化物溶液时,阳极上氯离子放电,根据溶液中氢离子或氢氧根离子浓度是否变化确定溶液pH是否变化,据此分析解答.
解答:
解:A.用石墨作电极电解NaOH溶液时,阳极上氢氧根离子放电、阴极上氢离子放电,所以实质上是电解水,NaOH的物质的量不变,溶液体积减小,则溶液中NaOH浓度增大,故A错误;
B.用石墨作电极电解H2SO4溶液时,阳极上氢氧根离子放电、阴极上氢离子放电,所以实质上是电解水,硫酸的物质的量不变,溶液体积减小,则溶液中硫酸浓度增大,故B错误;
C.用石墨电极电解硫酸钠溶液时,阳极上氢氧根离子放电、阴极上氢离子放电,所以实质上是电解水,硫酸钠的物质的量不变,溶液体积减小,硫酸钠的浓度增大,故C正确;
D.用石墨作电极电解NaCl溶液时,阳极上氯离子放电、阴极上氢离子放电,导致溶液中有氢氧根离子生成,则溶液中NaCl的物质的量在减少,NaCl溶液浓度将减小,故D错误;
故选C.
B.用石墨作电极电解H2SO4溶液时,阳极上氢氧根离子放电、阴极上氢离子放电,所以实质上是电解水,硫酸的物质的量不变,溶液体积减小,则溶液中硫酸浓度增大,故B错误;
C.用石墨电极电解硫酸钠溶液时,阳极上氢氧根离子放电、阴极上氢离子放电,所以实质上是电解水,硫酸钠的物质的量不变,溶液体积减小,硫酸钠的浓度增大,故C正确;
D.用石墨作电极电解NaCl溶液时,阳极上氯离子放电、阴极上氢离子放电,导致溶液中有氢氧根离子生成,则溶液中NaCl的物质的量在减少,NaCl溶液浓度将减小,故D错误;
故选C.
点评:本题考查了电解原理,明确离子放电顺序是解本题关键,根据电池反应式确定电解的本质,从而确定溶液浓度的变化,题目难度不大.

练习册系列答案
相关题目
用惰性电极电解下列溶液一段时间后,再加入一定量的某种纯净物(括号内物质),不能使溶液恢复到原来的成分和浓度的是( )
| A、KCl(HCl) |
| B、H2SO4(H2O) |
| C、AgNO3(HNO3) |
| D、CuSO4(CuCO3) |
小牧家里收藏了一件清代的铝制佛像,该佛像至今仍保存十分完好.该佛像未锈蚀的主要原因是( )
| A、铝的化学性质非常稳定,不易发生化学反应 |
| B、铝的氧化物容易发生还原反应 |
| C、铝被氧化生成一层致密的氧化膜薄膜 |
| D、铝的氧化物熔点很高 |
在下列反应中,水仅作还原剂的是( )
| A、Na2O+H2O=2NaOH |
| B、2F2+2H2O=4HF+O2 |
| C、Cl2+H2O=HCl+HClO |
| D、2K+2H2O=2KOH+H2↑ |
燃料充分燃烧的条件是( )
| A、有更高的温度 |
| B、有氧气参加 |
| C、达到着火点 |
| D、与空气有足够大的接触面 |
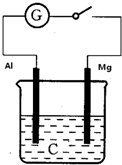 如图所示,把电极Al、Mg插入C的溶液中设计原电池.
如图所示,把电极Al、Mg插入C的溶液中设计原电池.
 是烯烃与H2加成的产物,则该烯烃可能有
是烯烃与H2加成的产物,则该烯烃可能有