题目内容
18.用铂电极电解Na2SO4溶液509.0g,阳极产生气体标况下为5.6L,此时电解质溶液的浓度变化是增大(填“增大”、“减小”、或“不变”),若要恢复到电解前状态需进行的操作是向电解后的溶液中加入9.0g蒸馏水.分析 用铂电极电解饱和Na2SO4溶液509.0g,阳极上是氢氧根离子失电子发生氧化反应,阴极上是氢离子得到电子发生还原反应生成氢气,电解过程中是电解水,溶液浓度增大,阳极产生气体标况下为5.6L为氧气,物质的量=$\frac{5.6L}{22.4L/mol}$=0.25mol,结合化学方程式定量计算得到电解减少的水,所以若要恢复到电解前状态需进行的操作是向电解后的溶液中加入对应减少的蒸馏水,
解答 解:用铂电极电解饱和Na2SO4溶液509.0g,阳极上是氢氧根离子失电子发生氧化反应,阴极上是氢离子得到电子发生还原反应生成氢气,电解过程中是电解水,溶液浓度增大,阳极产生气体标况下为5.6L为氧气,物质的量=$\frac{5.6L}{22.4L/mol}$=0.25mol,结合化学方程式定量计算得到电解减少的水为0.5mol,质量=0.5mol×18g/mol=9g,所以若要恢复到电解前状态需进行的操作是向电解后的溶液中加入9.0g蒸馏水,
故答案为:增大;向电解后的溶液中加入9.0g蒸馏水.
点评 本题考查了电解原理的分析应用,电解产物和溶液浓度的恢复,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
6.向35.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体完全反应,生成NO 和Cu(NO3)2.在所得溶液中加入1.0mol/L 的NaOH溶液1.3L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为49g.下列有关说法正确的是( )
| A. | Cu与Cu2O 的物质的量之比为2:1 | |
| B. | 硝酸的物质的量浓度为2.6mol/L | |
| C. | 产生的NO在标准状况下的体积为4.48L | |
| D. | Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
6.在4L密闭容器中充入6mol A气体和5mol B气体,在一定条件下发生反应:3A(g)+B(g)?2C(g)+xD(g),达到平衡时,生成了2mol C,经测定,D的浓度为0.5mol•L-1,下列判断正确的是( )
| A. | B的转化率为20% | |
| B. | 平衡时A的浓度为1.50 mol•L-1 | |
| C. | x=1 | |
| D. | 达到平衡时,在相同温度下容器内混合气体的压强是反应前的85% |
13.拟通过加入适量的化学试剂,采用恰当的分离混合物的方法,除去某溶液里溶解着的杂质,下列做法中不正确的是(括号内的物质为杂质)( )
| A. | NaCl溶液(BaCl2),加Na2SO4溶液,过滤 | |
| B. | KNO3溶液(AgNO3),加NaCl溶液,过滤 | |
| C. | NaCl溶液(碘),加汽油,分液 | |
| D. | KNO3溶液(碘),加四氯化碳,分液 |
3.下列化学用语正确的是( )
| A. | CO2的电子式: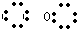 | B. | Mg2+的结构示意图: | ||
| C. | Na2O的电子式:Na+2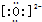 | D. | N2的结构式:N≡N |
10.无色透明的强酸性溶液中,能大量共存的离子组是( )
| A. | SiO32-、Br-、K+、Na+ | B. | NH4+、SO42-、Cl-、NO3- | ||
| C. | K+、Na+、ClO-、Cl- | D. | K+、SO42-、HCO3-、Mg2+ |
7.下列说法中,不正确的是( )
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②酒精灯加热铝箔至熔化,铝并不滴落,说明铝表面生成了一层致密的氧化膜
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④电解从海水中得到的氯化镁溶液可获得金属镁
⑤向蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性.
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②酒精灯加热铝箔至熔化,铝并不滴落,说明铝表面生成了一层致密的氧化膜
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④电解从海水中得到的氯化镁溶液可获得金属镁
⑤向蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性.
| A. | ①③④⑤ | B. | ②③④ | C. | ①③④ | D. | ①②③④⑤ |
8.下列有关离子组的评价及相关离子方程式均正确的是( )
| 选项 | 离子组 | 评价及离子方程式 |
| A | H+、Fe2+、NO3-、Cl- | 不能大量共存于同一溶液中,因为发生反应:Fe2++2H+=Fe3++H2↑ |
| B | Na+、K+、HCO3-、OH- | 不能大量共存于同一溶液中,因为发生反应:HCO3-+OH-=H2O+CO2↑ |
| C | Ca2+、NH4+、CO32-、Cl- | 能大量共存于同一溶液中 |
| D | Na+、NH4+、SO42-、Cl- | 能大量共存于同一溶液中 |
| A. | A | B. | B | C. | C | D. | D |