题目内容
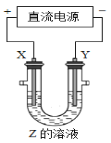
【题目】铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为:Fe3++Cr2+![]() Fe2++Cr3+。下列说法一定正确的是
Fe2++Cr3+。下列说法一定正确的是

A. 电池充电时,b极的电极反应式为:Cr3++e-=Cr2+
B. 电池放电时,b极的电极反应式为:Fe2+-e-=Fe3+
C. 电池放电时,Cl-从b极穿过选择性透过膜移向a极
D. 电池放电时,电路中每通过0.1 mol电子,Fe3+浓度降低0.1 mol·L-1
【答案】A
【解析】
A.充电时是电解池工作原理,阴极发生得电子的还原反应,电极反应式为Cr3++e-=Cr2+,A正确;
B.电池放电时,反应是原电池的工作原理,负极发生失电子的氧化反应,电极反应式为Cr2+-e-=Cr3+,B错误;
C.电池放电时,Cl-从正极室穿过选择性透过膜移向负极室,即从a极穿过选择性透过膜移向b极,C错误;
D.放电时,电路中每流过0.1mol电子,就会有0.1mol的铁离子得电子,减小浓度与体积有关,因此不能确定Fe3+浓度降低数值,D错误;
故合理选项是A。

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目