题目内容
9.下列反应的离子方程式中,书写正确的是( )| A. | 钠跟水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 向A12(SO4)3溶液中加入过量的氨水:A13++3NH3•H2O═A1(OH)3↓+3NH4+ | |
| C. | 向硫酸溶液中加入Ba(OH)2溶液:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| D. | FeCl2溶液跟Cl2反应:Fe2++Cl2═Fe3++2Cl- |
分析 A.电荷不守恒;
B.二者反应生成硫酸铵和氢氧化铝沉淀;
C.离子个数配比不符合物质结构组成;
D.电荷不守恒.
解答 解:A.钠跟水反应,离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.向A12(SO4)3溶液中加入过量的氨水,离子方程式:A13++3NH3•H2O═A1(OH)3↓+3NH4+,故B正确;
C.向硫酸溶液中加入Ba(OH)2溶液:,离子方程式:2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓,故C错误;
D.FeCl2溶液跟Cl2反应,离子方程式:2Fe2++Cl2═2Fe3++2Cl-,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,熟悉相关物质的性质及发生反应实质是解题关键,注意离子反应遵循客观事实、遵循电荷、原子个数守恒规律,题目难度不大.

练习册系列答案
相关题目
15.2010年8月至今年4月,浙江共查处酒后驾驶204 596起,其中醉酒驾驶20 593起,行政拘留20 471人.案件起数,居全国前列.交警执法时,主要测量驾驶员体内的( )
| A. | 醋酸 | B. | 乙醇 | C. | 甲醛 | D. | 葡萄糖 |
16.下列说法正确的是( )
| A. | 青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢铁 | |
| B. | 除去 CO2 中的 HCl 气体,只需将气体通过饱和的 Na2CO3 溶液 | |
| C. | 在某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明溶液中一定含 SO42- | |
| D. | 将 0.1mol/L 的 AlCl3 溶液 100mL 逐滴加到 0.1mol/L 的 NaOH 溶液 200ml 中与将 0.1mol/L 的 NaOH 溶液 200ml 逐滴加到 0.1mol/L 的 AlCl3溶液 100mL中,发生的现象和产生沉淀一样多 |
17.下列有关乙烯的说法中正确的是( )
| A. | 乙烯使溴水和酸性高锰酸钾溶液褪色原理相同 | |
| B. | 乙烯分子里所有原子都在同一个平面上,且碳氢键之间的键角约为 120° | |
| C. | 除去乙烷气体中的乙烯可以将混合气体通过盛有足量酸性高锰酸钾溶液的洗气瓶 | |
| D. | 乙烯和环丙烷(  )的分子组成符合通式 CnH2n,因此它们属于同系物 )的分子组成符合通式 CnH2n,因此它们属于同系物 |
4.在 pH=1 的溶液中,下列各组离子可能共存的是( )
| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、NO3-、HCO3- | ||
| C. | SO42-、Fe3+、K+、Cl- | D. | NO3-、K+、SO32-、Mg2+ |
14.在碘水中加入Na2SO3溶液,发现碘水褪色,这是由于发生了反应:Na2SO3+I2+H2O=Na2SO4+2HI,请据此分析:在含有Na2SO3、NaI、NaBr的混合液中通入一定量的氯气后,将溶液蒸干并充分灼烧,所得剩余固体的物质组成可能是( )
| A. | NaCl | B. | NaCl、NaBr、Na2SO4 | ||
| C. | NaCl、Na2SO4、I2 | D. | NaCl、NaI、Na2SO4 |
1.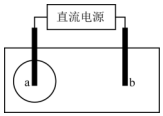 用两根铅笔芯接触饱和氯化钠溶液浸湿的试纸两端,接通直流电源.很短时间内,a电极与试纸接触处便宜出现一蓝色圆.下列说法正确的是( )
用两根铅笔芯接触饱和氯化钠溶液浸湿的试纸两端,接通直流电源.很短时间内,a电极与试纸接触处便宜出现一蓝色圆.下列说法正确的是( )
 用两根铅笔芯接触饱和氯化钠溶液浸湿的试纸两端,接通直流电源.很短时间内,a电极与试纸接触处便宜出现一蓝色圆.下列说法正确的是( )
用两根铅笔芯接触饱和氯化钠溶液浸湿的试纸两端,接通直流电源.很短时间内,a电极与试纸接触处便宜出现一蓝色圆.下列说法正确的是( )| A. | 该试纸可能是pH试纸,b电极为正极 | |
| B. | 该试纸可能是pH试纸,b电极处亦出现一蓝色圆 | |
| C. | 该试纸可能是淀粉碘化钾试纸,b电极附近溶液pH变小 | |
| D. | 该试纸可能是淀粉碘化钾试纸,b电极处发生还原反应 |
18.铁红(Fe2O3)常用作红色油漆和涂料.下列有关Fe2O3的叙述正确的是( )
| A. | 能跟盐酸反应 | B. | 可溶于水 | ||
| C. | 在空气中易被氧化 | D. | 有磁性 |
19.为了除去ZnCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,使溶液的pH升高,过滤后再向溶液中加入适量盐酸,这种试剂是( )
| A. | Fe | B. | K2CO3 | C. | KOH | D. | ZnCO3 |