题目内容
高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色非氯净水消毒剂和高容量电池材料。以粗FeO(含有CuO、Al2O3和SiO2等杂质)制备高铁酸钠的生产流程如下: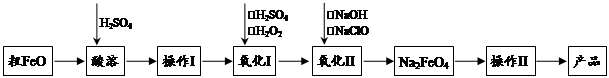
已知:NaClO不稳定,受热易分解。回答下列问题:
(1)高铁酸钠(Na2FeO4)中铁元素的化合价为 。
粗FeO酸溶过程中通入高温水蒸气,其目的是 。
(2)操作Ⅰ目的是得到高纯度FeSO4溶液,氧化Ⅰ后的溶液中如果滴加KSCN溶液,溶液变为血红色,由此推测氧化Ⅰ反应的离子方程式为 。
(3)本工艺中需要高浓度NaClO溶液,可用Cl2与NaOH溶液反应制备:
①Cl2与NaOH溶液反应的化学方程式为_____________________________________。
②在不同温度下进行该反应,反应相同一段时间后,测得生成NaClO浓度如下:
| 温度/0C | 15 | 20 | 25 | 30 | 35 | 40 | 45 |
| NaClO浓度/mol·L-1 | 4.6 | 5.2 | 5.4 | 5.5 | 4.5 | 3.5 | 2 |
_______________________________________________________________________________________。
(1) +6 升高温度加快反应速率(或 提高酸溶效率)
(2)2Fe2++H2O2+2H+=2Fe3++2H2O(没配平扣1分)
(3)①Cl2+2NaOH=NaCl+NaClO+H2O(写成离子方程式不扣分)
②规律:NaClO浓度随温度升高而降低(或减小)。
原因(共2分):温度小于30℃时,升高温度,反应速率增大(1分);温度高于30℃时, NaClO不稳定而分解。(1分)(多答其他不扣分)
解析试题分析:据化合价代数和为零算出铁的化合价为正六价。水不参与反应,所以只能从温度方面进行考虑加入高温水的目的即加快反应速率。三价的铁离子遇到硫氰化钾会显红色,所以据现象可推出2Fe2++H2O2+2H+=2Fe3++2H2O ,氯气与碱反应会生成两种盐,一种是正盐。另一种是次氯酸盐。故Cl2+2NaOH=NaCl+NaClO+H2O 从表框上看,30摄氏度之前,反应速率是随着温度的增加而逐渐增大的,主要考虑到增大温度,反应速率加快。30摄氏度之后,次氯酸的量逐渐减小主要是考虑,次氯酸是不稳定的,在高温下会分解。
考点:主要考查金属元素与非金属元素的综合应用

将锌、铁、铜粉末按一定比例混合投入到一定量的硝酸中,微热,充分反应后过滤,弃去滤渣,滤液中金属阳离子情况不可能是
| A.只含Cu2+、Fe2+、Zn2+ | B.只含Zn2+ |
| C.只含Fe2+、Zn2+ | D.只含Cu2+、Fe3+、Zn2+ |
(15分)用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/LFeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压值:)
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| I | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| II | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| III | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(2)I中,Fe2+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应的方程式_____。
(3)由II推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有_____性。
(4)II中虽未检测出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| IV | a>x≥c | 无明显变化 | 有Cl2 |
| V | c>x≥b | 无明显变化 | 无Cl2 |
②IV中检测Cl2的实验方法:____________________。
③与II对比,得出的结论(写出两点):___________________。



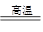 2Cu + SO2
2Cu + SO2 FeSO4 + Cu
FeSO4 + Cu
 原理,用下列仪器(加热及固定装置省略)制备干燥、纯净的CO,并用CO还原CuO粉末。
原理,用下列仪器(加热及固定装置省略)制备干燥、纯净的CO,并用CO还原CuO粉末。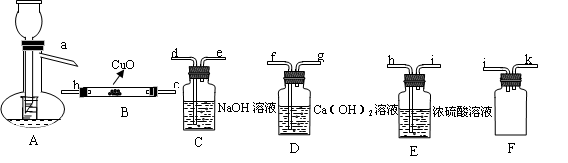
 2 Cu2O + O2↑;③ Cu2O +2H+
2 Cu2O + O2↑;③ Cu2O +2H+