题目内容
某化学兴趣小组在实验室模拟FeCl2转化为FeCl3的过程.同时检验氯气的部分性质.装置如图所示.请回答:
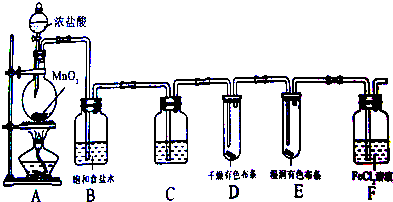
(1)A中发生反应的化学方程式为 .
(2)D、E中的现象为 .
(3)装置B的作用是
(4)请你简要评价该套实验装置 .

(1)A中发生反应的化学方程式为
(2)D、E中的现象为
(3)装置B的作用是
(4)请你简要评价该套实验装置
考点:氯气的实验室制法,氯、溴、碘的性质实验
专题:实验题
分析:(1)实验室用二氧化锰与浓盐酸反应制备氯气;
(2)依据干燥的有色布条不褪色,湿润的有色布条褪色,对比说明具有漂白性的不是氯气;
(3)装置B为饱和氯化钠溶液,用来除去挥发出的氯化氢气体,减小氯气在水中的溶解度;
(4)氯气有毒,排放到空气中会污染空气,实验装置中无尾气吸收装置.
(2)依据干燥的有色布条不褪色,湿润的有色布条褪色,对比说明具有漂白性的不是氯气;
(3)装置B为饱和氯化钠溶液,用来除去挥发出的氯化氢气体,减小氯气在水中的溶解度;
(4)氯气有毒,排放到空气中会污染空气,实验装置中无尾气吸收装置.
解答:
解:(1)A.二氧化锰与浓盐酸反应生成氯化锰、水、氯气,方程式为:MnO2+4HCl
MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl
MnCl2+Cl2↑+2H2O;
(2)干燥的有色布条不褪色,湿润的有色布条褪色,说明具有漂白性的不是氯气,而是次氯酸,
故答案为:干燥的有色布条不褪色,湿润的有色布条褪色;
(3)装置B为饱和氯化钠溶液,用来除去挥发出的氯化氢气体,减小氯气在水中的溶解度;
故答案为:吸收氯气中的氯化氢杂质气体,减小氯气的溶解度;
(4)氯气有毒,排放到空气中会污染空气,实验装置中无尾气吸收装置,会造成环境污染;
故答案为:无尾气吸收装置,会造成环境污染.
| ||
故答案为:MnO2+4HCl
| ||
(2)干燥的有色布条不褪色,湿润的有色布条褪色,说明具有漂白性的不是氯气,而是次氯酸,
故答案为:干燥的有色布条不褪色,湿润的有色布条褪色;
(3)装置B为饱和氯化钠溶液,用来除去挥发出的氯化氢气体,减小氯气在水中的溶解度;
故答案为:吸收氯气中的氯化氢杂质气体,减小氯气的溶解度;
(4)氯气有毒,排放到空气中会污染空气,实验装置中无尾气吸收装置,会造成环境污染;
故答案为:无尾气吸收装置,会造成环境污染.
点评:本题考查了氯气的制备和性质的检验,题目综合性较强,难度中等,

练习册系列答案
相关题目
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( )
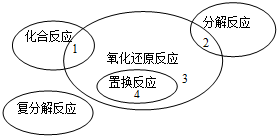

| A、4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||||
B、2NaHCO3
| ||||
C、CH4+2O2
| ||||
| D、Cl2+2KBr═Br2+2KCl |
下列说法正确的是( )
| A、冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物 |
| B、“血液透析”利用了胶体的性质 |
| C、“PM2.5”是细小颗粒物悬浮在空气中形成胶体,严重危害人体健康 |
| D、电解质在水溶液和熔融状态下均能导电 |
下列实验事故的处理方法正确的是( )
| A、实验桌上的酒精灯倾倒了燃烧起来,马上用湿布扑灭 |
| B、不慎将酸或碱液溅入眼内,应立即闭上眼睛,用手揉擦 |
| C、手上不慎溅有少量浓硫酸,赶紧找抹布用力拭去 |
| D、配制硫酸溶液时,先在量筒中加入一定体积的水,再边搅拌边慢慢加入浓硫酸 |

 按要求对如图中两极进行必要的连接并填空:
按要求对如图中两极进行必要的连接并填空:
