题目内容
如下图,已知:
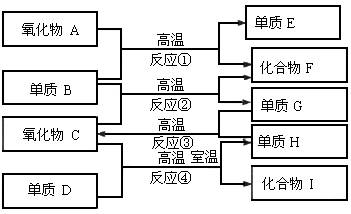
①单质E可作为半导体材料;
②化合物F是不能生成盐的氧化物;
③化合物I能溶于水呈酸性,它能够跟氧化物A起反应。
据此,请填空:
(1)化合物F是__________;
(2)化合物I是__________;
(3)反应③的化学方程式是___________;
(4)反应④的化学方程式是___________。
答案:
解析:
解析:
解析 本题考查元素及其化合物的性质,属常规“方框图”题型。在全面系统掌握元素及其化合物性质的基础上,要善于抓住某些元素的特殊性质作为“切入点”,找到解题的突破口。比如,本题一开始就指出单质E和化合物F分别是半导体材料和不形成盐的氧化物,因而它们的首选答案可考虑各为Si和CO,于是,反应①的化学方程式应为: SiO2+2C 答案:(1)CO(一氧化碳);(2)HF(氟化氢); (3)3H2+O2
|

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目

 回答下列问题:
回答下列问题:


 A为只含有C、H、O三种元素的芳香烃衍生物,各物质间的相互转化关系如下图.已知:ROH+HX
A为只含有C、H、O三种元素的芳香烃衍生物,各物质间的相互转化关系如下图.已知:ROH+HX