题目内容
3.下列各组物质的晶体中,化学键类型和晶体类型都相同的是( )| A. | CO2和H2S | B. | KOH和CH4 | C. | Si和CO2 | D. | NaCl和HCl |
分析 一般类说,非金属之间形成共价键,活泼金属与非金属形成离子键,含离子键的为离子晶体,含共价键的可能为分子晶体或原子晶体,以此来解答.
解答 解:A.CO2和H2S均含共价键,由分子构成,均为分子晶体,故A选;
B.KOH含离子键和共价键,为离子晶体,而CH4含共价键,为分子晶体,故B不选;
C.Si含共价键,为原子晶体,而CO2含含共价键,为分子晶体,故C不选;
D.NaCl含离子键,为离子晶体,HCl含共价键,为分子晶体,故D不选;
故选A.
点评 本题考查化学键及晶体类型,为高频考点,把握化学键的形成及判断为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键及晶体类型的判断,题目难度不大.

练习册系列答案
相关题目
13.糖类、油脂和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是( )
| A. | 蛋白质中至少含有四种元素 | |
| B. | 用饱和的CuSO4溶液使蛋清液发生盐析,进而分离、提纯蛋白质 | |
| C. | 所有的糖类、油脂和蛋白质均能发生水解反应 | |
| D. | 油脂在稀硫酸催化条件下的水解又叫皂化反应 |
14.下列物质在氢氧化钠溶液和加热条件下反应后生成的对应有机物中,不能够能被催化氧化成醛的是( )
| A. | (CH3)2CHCH2Cl | B. | CH3C(CH3)2I | C. | (CH3)3COOCH2CH3 | D. | CH3C(CH3)2CH2Br |
11.在恒温恒容条件下,2NO+O2?2NO2达到平衡的标志是( )
| A. | NO、O2、NO2分子数目比是2:1:2 | |
| B. | 反应混合物中各组分物质的浓度相等 | |
| C. | 混合气体的总质量不变 | |
| D. | 混合气体的平均相对分子质量不变 |
12.下列物质中只含有离子键的是( )
| A. | CS2 | B. | Na2O2 | C. | CaO | D. | CH3COOH |
13.下列物质中,不属于通常所说的三大合成材料的是( )
| A. | 塑料 | B. | 蛋白质 | C. | 合成纤维 | D. | 合成橡胶 |
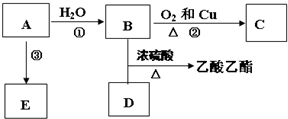
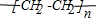 ,E不能(填“能”或“不能”)使酸性KMnO4溶液褪色.
,E不能(填“能”或“不能”)使酸性KMnO4溶液褪色.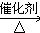 2CH3CHO+2H2O,反应类型氧化反应;B+DCH3COOH+C2H5OH
2CH3CHO+2H2O,反应类型氧化反应;B+DCH3COOH+C2H5OH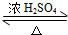 CH3COOC2H5+H2O,反应类型酯化(或取代)反应.
CH3COOC2H5+H2O,反应类型酯化(或取代)反应.
