题目内容
关于氮族元素的性质,下列推断错误的是( )
| A、最高价氧化物为R2O5,其水化物化学式为HRO3或H3RO4 |
| B、非金属性:磷>砷,气态氢化物的还原性:PH3>AsH3 |
| C、最高价含氧酸的酸性:硒酸>砷酸>锗酸 |
| D、所形成的氢化物中BiH3最不稳定 |
考点:同一主族内元素性质递变规律与原子结构的关系
专题:元素周期律与元素周期表专题
分析:A.N元素最高价氧化物的水化物是HRO3;
B.元素非金属性越强,其气态氢化物越稳定;
C.同一周期元素,元素非金属性随着原子序数增大而增强,元素非金属性越强,其最高价含氧酸酸性越强;
D.元素非金属性越强,其气态氢化物越稳定.
B.元素非金属性越强,其气态氢化物越稳定;
C.同一周期元素,元素非金属性随着原子序数增大而增强,元素非金属性越强,其最高价含氧酸酸性越强;
D.元素非金属性越强,其气态氢化物越稳定.
解答:
解:A.N元素最高价氧化物为N2O5,其水化物化学式为HNO3,故A错误;
B.非金属性P>As,气态氢化物的还原性PH3>AsH3,故B正确;
C.非金属性Se>As>Ge,所以其最高价氧化物的水化物酸性:硒酸>砷酸>锗酸 ,故C正确;
D.氮族元素中非金属性最弱的是Bi元素,则气态氢化物最不稳定的是BiH3,故D正确;
故选A.
B.非金属性P>As,气态氢化物的还原性PH3>AsH3,故B正确;
C.非金属性Se>As>Ge,所以其最高价氧化物的水化物酸性:硒酸>砷酸>锗酸 ,故C正确;
D.氮族元素中非金属性最弱的是Bi元素,则气态氢化物最不稳定的是BiH3,故D正确;
故选A.
点评:本题考查同一主族元素性质的递变规律,明确同一主族元素非金属性强弱、非金属的非金属性强弱与其气态氢化物的稳定性和其最高价含氧酸的酸性强弱的关系即可解答,题目难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
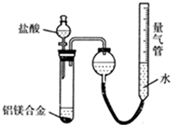 如图,某镁铝合金中,镁与铝物质的量之比为1:1,将两份质量相等的镁铝合金分别与足量的盐酸、NaOH溶液反应,生成气体的物质的量之比为( )
如图,某镁铝合金中,镁与铝物质的量之比为1:1,将两份质量相等的镁铝合金分别与足量的盐酸、NaOH溶液反应,生成气体的物质的量之比为( )| A、2:3 | B、3:2 |
| C、5:3 | D、3:5 |
进行一氯取代反应后,生成的一氯代物有两种结构的是( )
| A、乙烷 |
| B、新戊烷 |
| C、2,3-二甲基丁烷 |
| D、2,2,3,3-四甲基丁烷 |
下列混合物可用加热的方法分离的是( )
| A、碘和氯化铵 |
| B、碳酸氢钠和二氧化锰 |
| C、硫酸钾和氯酸钾 |
| D、氯化铵和氯化钡 |
某课外小组欲测定过氧化钠与碳酸钠混合物中过氧化钠的质量分数,准确称量a克样品,下列后续实验方案中,不合理的是( )
| A、隔绝空气加热,冷却后,称量剩余固体质量m1 g |
| B、与足量稀盐酸反应并蒸干,称量剩余固体质量m2 g |
| C、与足量水反应并加热,收集到标准状况下V1 L干燥气体 |
| D、与足量稀硫酸反应并加热,收集到标准状况下V2 L 干燥气体 |
用铜作催化剂,使1-丙醇氧化为某有机物,下列物质中,与该有机物互为同分异构体的是( )
| A、CH3OCH2CH3 |
| B、CH3CH(OH)CH3 |
| C、CH3COCH3 |
| D、CH3COOCH3 |
下列关于金属Na的叙述中,说法正确的是( )
| A、Na在空气中燃烧,发出黄色火焰 |
| B、Na在空气中燃烧,产物是Na2O |
| C、Na是银白色金属,硬度大,熔点高 |
| D、Na、Cu合金可作原子反应堆的导热剂 |
某有机物A的结构简式为 取Na、NaOH和Cu(OH)2分别与等物质的量的A在一定条件下充分反应时,理论上需Na、NaOH和Cu(OH)2三种物质的物质的量之比为( )
取Na、NaOH和Cu(OH)2分别与等物质的量的A在一定条件下充分反应时,理论上需Na、NaOH和Cu(OH)2三种物质的物质的量之比为( )
 取Na、NaOH和Cu(OH)2分别与等物质的量的A在一定条件下充分反应时,理论上需Na、NaOH和Cu(OH)2三种物质的物质的量之比为( )
取Na、NaOH和Cu(OH)2分别与等物质的量的A在一定条件下充分反应时,理论上需Na、NaOH和Cu(OH)2三种物质的物质的量之比为( )| A、2:2:1 |
| B、4:2:1 |
| C、2:1:2 |
| D、1:1:1 |
下列物质中,能导电是( )
| A、氯化钠晶体 |
| B、澄清石灰水 |
| C、酒精 |
| D、CO2 |