��Ŀ����
��7�֣�ij�¶���1���ܱ������м���1.5molN2��4.5molH2,ʹ��ӦN2+3H2 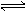 2NH3��ƽ�⣬ ���ƽ��������N2��H2��NH3�ֱ�Ϊm��n��gmol������¶Ȳ���ֻ�ı��ʼʱ�����ʵļ�����������ƽ��ʱm��n��gֵ���䣬��N2��H2��NH3��������x��y��z��ʾ��Ӧ����������
2NH3��ƽ�⣬ ���ƽ��������N2��H2��NH3�ֱ�Ϊm��n��gmol������¶Ȳ���ֻ�ı��ʼʱ�����ʵļ�����������ƽ��ʱm��n��gֵ���䣬��N2��H2��NH3��������x��y��z��ʾ��Ӧ����������
����x=0��y=0, ��z= mol��
����x=0.75mol, ��y= mol, z= mol��
��Ӧ�����һ�������� �� ��
(����������ʽ��ʾ������һ��ֻ��x��z����һ��ֻ��y��z)
�� z= 3 mol��
�� y= 2.25 mol, z= ��.�� mol��
��Ӧ�����һ�������� x+z/2=��.�� �� y+3z/2=4.5 ��

��ϰ��ϵ�д�
�����Ŀ
 pC��g��+qD��S����H��0��ͼij��Ӧ�����и��������ʵ���n��mol����ʱ��t�ı仯����ͼ��
pC��g��+qD��S����H��0��ͼij��Ӧ�����и��������ʵ���n��mol����ʱ��t�ı仯����ͼ��

 Si(s)+2CO(g)
Si(s)+2CO(g)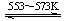 SiHCl3(l)��H2(g) + Q��Q��0��
SiHCl3(l)��H2(g) + Q��Q��0�� Si(��)��3HCl(g)
Si(��)��3HCl(g)