题目内容
18.硅与金刚砂(SiC)是两种重要的工业产品,它们都可由二氧化硅与碳反应制得,反应关系如图1所示:
(1)基态硅原子核外未成对的电子数为2;Si与C相比,第一电离能较小的是Si(填元素符号).
(2)由SiO2生成SiC的化学方程式是SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑.
(3)粗硅提纯过程中往往会生成四氯化硅(SiCl4),该物质在常温常压下为无色液体,其中Si原子的杂化轨道类型是sp3,Cl-Si-Cl键的键角为109°28′.
(4)SiC晶体与晶体硅(结构如图甲所示)的结构相似,其中C原子和Si原子的位置是交替的,在SiC中最小的环上有6个原子,SiC与晶体硅相比,SiC熔点较高.原因是二者均为原子晶体,结构和组成类似,Si-Si键键长大于Si-C键键长,故Si-Si键键能小,导致晶体硅的熔点低于碳化硅.
(5)SiC晶胞如图乙所示,Si-C键的键能为a kJ•mol-1,理论上分解1mol SiC形成气态的原子所需要的能量为4akJ(用含a的式子表示).
分析 (1)根据核外电子排布规则判断,同主族从上到下第一电离能逐渐减小;
(2)依据图示可知X为CO,SiO2和焦炭反应生成碳化硅和CO;
(3)根据四氯化硅中Si原子的价层电子对数判断杂化类型和键角;
(4)晶体硅中最小的为六元环,含有6个原子,SiC与硅晶体相似,因此也含有6个原子;原子晶体熔沸点的高低取决于共价键的稳定性;
(5)依据晶胞计算方法计算即可.
解答 解:(1)基态Si原子电子排布式为1s22s22p63s23p2,则基态硅原子核外未成对的电子数为2,同主族自下而上第一电离能逐渐减小,因此第一电离能:C>Si,
故答案为:2;Si;
(2)SiO2和焦炭反应生成碳化硅和CO,化学方程式为:SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO;
故答案为:SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO;
(3)SiCl4中Si原子的价层电子对数为4+$\frac{1}{2}$(4-4×1)=4,没有孤电子对,硅原子采用sp3杂化,为正四面体结构,故Cl-Si-Cl键的键角为109°28′;
故答案为:sp3;109°28′;
(4)晶体硅中最小的为六元环,含有6个原子,SiC与硅晶体相似,因此也含有6个原子,两者都是原子晶体,结构和组成相似,Si-Si键长大于Si-C键长,Si-Si键能小,晶体硅的熔沸点低于碳化硅,
故答案为:6;二者均为原子晶体,结构和组成类似,Si-Si键键长大于Si-C键键长,故Si-Si键键能小,导致晶体硅的熔点低于碳化硅;
(5)SiC中,C位于顶点和面心,故C为:8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,Si位于晶胞的中心,故Si为4,那么该晶胞即为Si4C4,即l mol SiC中含有4mol共价键,故分解l mol SiC形成气态原子所需要的能量为4akJ,
故答案为:4a.
点评 本题考查化学方程式的书写和电子排布规律、第一电离能、化学键、杂化类型、分子结构和空间构型、晶胞计算等知识,综合性强,为物质结构常规考题形式,题目难度中等.

| A. | 汽油 | B. | 纯植物油 | C. | 蔗糖 | D. | 聚乙烯 |
 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H1=+49.0kJ•mol-1
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H2=-192.9kJ•mol-1
下列说法正确的是( )
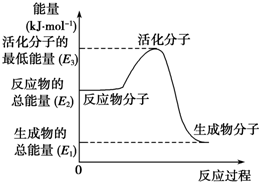
| A. | 上述图示的反应为吸热反应 | |
| B. | 图中的能量变化如图所示,则△H=E1-E3 | |
| C. | H2燃烧能放出大量的热,故CH3OH转变成H2的过程必须吸收热量 | |
| D. | 根据①②推知:在25℃、101 kPa时,1 mol CH3OH(g)完全燃烧生成CO2和H2O放出的热量应大于676.7 kJ |
 X、Y、Z、J、Q、W六种元素,原子序数依次增大,其中X、Y、Z、J、Q是短周期主族元素.元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3:8,X能与J形成离子化合物,且J+的半径大于X-的半径,Y的氧化物是形成酸雨的主要物质之一.W是应用最广泛的金属元素.请回答:
X、Y、Z、J、Q、W六种元素,原子序数依次增大,其中X、Y、Z、J、Q是短周期主族元素.元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3:8,X能与J形成离子化合物,且J+的半径大于X-的半径,Y的氧化物是形成酸雨的主要物质之一.W是应用最广泛的金属元素.请回答:(1)Y元素原子的结构示意图为
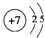 .
.(2)元素的金属性J>W(填“>”或“<”),下列各项中,能说明这一结论的事实有ACD(填序号)
A.单质与酸反应置换出氢气的难易程度 B.单质的熔点
C.最高价氧化物对应水化物的碱性强弱 D.在金属活动顺序表中的位置
(3)已知:①3W(s)+2Z2(g)=W3Z4(s)△H1=-1118.4kJ/mol
②2X2(g)+Z2(g)=2X2Z(g)△H2=-483.8kJ/mol
则反应3W(s)+4X2Z(g)=W3Z4(s)+4X2(g)的△H=-150.8kJ/mol.
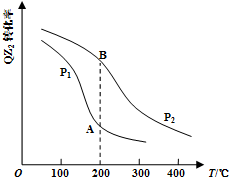
(4)已知反应:2QZ2(g)+Z2(g)?2QZ3(g),QZ2的平衡转化率与温度、压强的关系如图所示:
①压强:P1<P2(填“>”、“=”或“<”).
②200℃下,将一定量的QZ2和Z2充入体积不变的密闭容器中,经10min后测得容器中各物质的物质的量浓度如下表所示:
| 气体 | QZ2 | Z2 | QZ3 |
| 浓度(mol/L) | 0.4 | 1.2 | 1.6 |
a.反应速率v(QZ2)=v(QZ3)
b.体系的压强保持不变
c.混合气体的密度保持不变
d.QZ2和Z2的体积比保持不变
计算上述反应在0~10min内,v(QZ2)=0.16mol/(L.min).
(5)以YX3为燃料可以设计成燃料电池(电极材料均为惰性电极,KOH溶液作电解质溶液)该电池负极电极反应式为2NH3-6e-+6OH-=N2+6H2O.
| A. | 离子化合物中只能含离子键,不能有共价键 | |
| B. | 所有非金属之间形成的化学键一定是共价键 | |
| C. | 电子数相同的两种微粒一定是同一元素 | |
| D. | 化学变化一定有化学键的断裂和形成 |
| A. | 肯定有O2 | B. | 肯定只有NH3和NO | ||
| C. | 肯定有NH3、NO、HCl | D. | 肯定没有Cl2、NH3、NO2 |
 .
. .
. .
.