题目内容
7.元素周期表中第 VIIA族元素的单质及其化合物的用途广泛.(1)与氯元素同族的短周期元素的原子结构示意图为
 .
.(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是bc(填序号).
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:NaCl溶液 $→_{I}^{80℃通电}$ NaClO3溶液$→_{II}^{室温KCl}$ KClO3晶体
①完成 I中反应的总化学方程式:NaCl+3H2O=NaClO3+3H2
②II中反应过程能析出KClO3晶体而无其它晶体析出的原因是室温下,氯酸钾在水中的溶解度明显小于其它晶体.
(4)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1.写出该反应的化学方程式:4KClO3$\frac{\underline{\;400℃\;}}{\;}$KCl+3KClO4.
(5)已知:将Cl2通人适量KOH溶液,产物中可能有KC1、KClO、KC1O3,且$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$ 的值与温度高低有关.当n(KOH)=a mol时,下列有关说法正确的是①②③
①若某温度下,反应后$\frac{c(Cl{O}^{-})}{c(Cl{O}_{3}^{-})}$=11,则溶液中且且$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=$\frac{1}{2}$
②参加反应的氯气的物质的量等于$\frac{1}{2}$a mol
③改变温度,反应中转移电子的物质的量ne的范围:$\frac{1}{2}$a mol≤ne≤$\frac{5}{6}$a mol
④改变温度,产物中KC1O3的最大理论产量为$\frac{1}{7}$a mol.
分析 (1)与氯元素同族的短周期元素是F元素,根据原子结构示意图来回答;
(2)同一主族元素,元素的非金属性越强,其氢化物的稳定性越强、其最高价氧化物的水化物酸性越强、其单质的氧化性越强,据此判断;
(3)①电解时,阳极上氯离子放电生成氯酸根离子、阴极上氢离子放电生成氢气;
两种化合物相互交换成分生成另外的两种化合物的反应为复分解反应,相同温度下,溶解度小的物质先析出;
(4)根据题干信息判断该无氧酸盐为氯化钾,再根据化合价变化判断另一种无氧酸盐名称,最后根据化合价升降相等配平即可;
(5)①设n(ClO-)=1mol,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则n(Cl-)=11mol,根据电子转移守恒计算n(ClO3-),据此计算判断;
②由Cl原子守恒可知,2n(Cl2)=n(KCl)+n(KClO)+n(KClO3),由钾离子守恒可知n(KCl)+n(KClO)+n(KClO3)=n(KOH);
③氧化产物只有KClO3时,转移电子最多,氧化产物只有KClO时,转移电子最少,根据电子转移守恒及钾离子守恒计算;
④氧化产物只有KClO3时,其物质的量最大,结合③中计算判断.
解答 解:(1)与氯元素同族的短周期元素是F元素,原子结构示意图位: ,故答案为:
,故答案为: ;
;
(2)a.Cl2、Br2、I2的熔点与分子间作用力有关,与非金属性无关,故a错误;
b.单质的氧化性越强,则非金属性越强,可以根据Cl2、Br2、I2的氧化性来判断非金属性,故b正确;
c.氢化物的稳定性越强,则非金属性越强,可以根据HCl、HBr、HI的热稳定性来判断非金属性,故c正确;
d.不能根据HCl、HBr、HI的酸性强弱来判断元素的非金属性,故d错误;
故答案为:bc;
(3)①电解时,阳极上氯离子放电生成氯酸根离子、阴极上氢离子放电生成氢气,所以反应方程式为NaCl+3H2O═NaClO3+3H2↑,
故答案为:NaCl+3H2O=NaClO3+3H2;
②NaClO3转化为KClO3,说明该反应中两种物质相互交换离子生成盐,为复分解反应,相同温度下,溶解度小的物质先析出,室温下KClO3在水中的溶解度明显小于其它晶体,所以先析出KClO3,
故答案为:室温下KClO3在水中的溶解度明显小于其它晶体;
(4)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1,则该无氧酸为KCl,KCl中氯元素化合价为-1,说明氯酸钾中氯元素化合价降低,则另一种含氧酸盐中氯元素化合价会升高,由于氯酸钾中氯元素化合价为+5,则氯元素化合价升高只能被氧化成高氯酸钾,根据氧化还原反应中化合价升降相等配平该反应为:4KClO3$\frac{\underline{\;400℃\;}}{\;}$KCl+3KClO4,故答案为:4KClO3$\frac{\underline{\;400℃\;}}{\;}$KCl+3KClO4.
(5)①设n(ClO-)=1mol,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则n(Cl-)=11mol,电子转移守恒,5×n(ClO3-)+1×n(ClO-)=1×n(Cl-),即:5×n(ClO3-)+1×1mol=1×11mol,解得:n(ClO3-)=2mol,故溶液中$\frac{c(Cl{O}^{-})}{c(Cl{{O}_{3}}^{-})}$=$\frac{1}{2}$,故正确;
②由Cl原子守恒可知,2n(Cl2)=n(KCl)+n(KClO)+n(KClO3),由钾离子守恒可知n(KCl)+n(KClO)+n(KClO3)=n(KOH),故参加反应的氯气的物质的量为:n(Cl2)=$\frac{1}{2}$n(KOH)=0.5a mol,故正确;
③氧化产物只有KClO3时,转移电子最多,根据电子转移守恒n(KCl)=5(KClO3),由钾离子守恒:n(KCl)+n(KClO3)=n(KOH),故n(KClO3)=$\frac{1}{6}$n(KOH)=$\frac{1}{6}$a mol,转移电子最大物质的量为:$\frac{1}{6}$a mol×5=$\frac{5}{6}$a mol,氧化产物只有KClO时,转移电子最少,根据电子转移守恒n(KCl)=n(KClO),根据钾离子守恒:n(KCl)+n(KClO)=n(KOH),故:n(KClO)=$\frac{1}{2}$n(KOH)=$\frac{1}{2}$a mol,转移电子最小物质的量=$\frac{1}{2}$a mol×1=$\frac{1}{2}$a mol,则反应中转移电子的物质的量ne的范围为:$\frac{1}{2}$a mol≤ne≤$\frac{5}{6}$a mol,故正确;
④氧化产物只有KClO3时,其物质的量最大,由C中计算可知:n最大(KClO3)=$\frac{1}{6}$n(KOH)=$\frac{1}{6}$a mol,故错误;
故选①②③.
点评 本题考查较综合,涉及同一周期中元素周期律与原子结构的关系、化学方程式的书写、氧化还原反应计算等知识,注重高频考点的考查,题目难度较大,有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

| A. | ①②③ | B. | ③④⑤ | C. | ②③⑤ | D. | ①③⑤ |

| A. | NPG与乙二醇互为同系物 | |
| B. | 1mol该醇与足量的钠反应放出1mol H2 | |
| C. | NPG一定条件下能发生取代反应、酯化反应、氧化反应、加成反应、加聚反应 | |
| D. | 分子式为C5H12O2 |
①Cl2+2KBr═2KCl+Br2,②KClO3+6HCl═3Cl2+KCl+3H2O,③2KBrO3+Cl2═Br2+2KClO3,
下列说法正确的是.
| A. | 上述三个反应都有单质生成,所以都是置换反应 | |
| B. | 氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2 | |
| C. | 反应②中还原剂与氧化剂的物质的量之比为6:1 | |
| D. | ③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol |
| A. | Ca(ClO)2、KAl(SO4)2﹒12H2O | B. | Cl2、KAl(SO4)2﹒12H2O | ||
| C. | H2O、SO2 | D. | H2SO4、亚硫酸钠 |
| A. | 核内无中子的原子 | |
| B. | 价电子构型为3s23p1 | |
| C. | 最外层电子数等于倒数第三层上的电子数的原子 | |
| D. | N层上无电子,最外层上的电子数等于电子层数的原子 |
| A. | Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 将少量铜屑放入浓硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| C. | 过量的二氧化碳通入“水玻璃”中:CO2+SiO32-+H2O═CO32-+H2SiO3↓ | |
| D. | Cl2通入NaOH稀溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
 C.CH3CH═CHCH2OH D.
C.CH3CH═CHCH2OH D.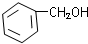
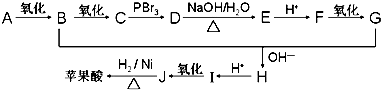
 .
.


 +n HO-CH2CH2-OH$\stackrel{一定条件}{→}$
+n HO-CH2CH2-OH$\stackrel{一定条件}{→}$ +(2n-1)H2O
+(2n-1)H2O 、
、 .
.