题目内容
下列实验中,所采取的分离方法与对应原理都正确的是( )
| 选项 | 目的 | 分离方法 | 原理 |
| A. | 二氧化碳中混有的少量一氧化碳 | 通入适量氧气点燃 | 一氧化碳会燃烧成二氧化碳 |
| B. | 除去鸡蛋清胶体中混的杂质NaCl | 过滤 | 鸡蛋清胶体不能通过滤纸 |
| C. | 除去KNO3固体中混杂的NaCl | 重结晶 | NaCl在水中的溶解度很大 |
| D. | 除去BaSO4粉末中的BaCO3 | 盐酸溶解过滤洗涤 | 盐酸可溶BaCO3,不溶BaSO4 |
| A、A | B、B | C、C | D、D |
考点:物质的分离、提纯和除杂
专题:实验评价题
分析:A.二氧化碳含量多,CO不能燃烧;
B.胶体和离子均可透过滤纸;
C.应利用二者溶解度随温度的变化不同分离;
D.盐酸可溶解BaCO3,不溶解BaSO4,则加盐酸溶解、过滤即可.
B.胶体和离子均可透过滤纸;
C.应利用二者溶解度随温度的变化不同分离;
D.盐酸可溶解BaCO3,不溶解BaSO4,则加盐酸溶解、过滤即可.
解答:
解:A.二氧化碳含量多,CO不能燃烧,不能除杂,应利用气体通过灼热的CuO来除杂,故A错误;
B.胶体和离子均可透过滤纸,则不能利用过滤法分离,应选择渗析法,故B错误;
C.根据二者在水中随温度升高而溶解度不同,利用重结晶法.NaCl随温度升高溶解度变化不大,KNO3随温度升高溶解度变化大,经冷却过滤,故C错误;
D.盐酸可溶解BaCO3,不溶解BaSO4,则加盐酸溶解、过滤即可得到纯净的硫酸钡,故D正确.
故选D.
B.胶体和离子均可透过滤纸,则不能利用过滤法分离,应选择渗析法,故B错误;
C.根据二者在水中随温度升高而溶解度不同,利用重结晶法.NaCl随温度升高溶解度变化不大,KNO3随温度升高溶解度变化大,经冷却过滤,故C错误;
D.盐酸可溶解BaCO3,不溶解BaSO4,则加盐酸溶解、过滤即可得到纯净的硫酸钡,故D正确.
故选D.
点评:本题考查混合物分离提纯,为高频考点,把握物质的性质及性质差异、发生的反应等为解答的关键,注重分析与实验能力的考查,题目难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
通常情况下,下列各组物质能够共存且能用碱石灰或浓硫酸来干燥的气体是( )
| A、NH3、N2、H2 |
| B、HCl、NH3、CO2 |
| C、H2、O2、N2 |
| D、SO2、H2S、O2 |
下列实验操作正确的是( )
| A、玻璃仪器外壁有水可以直接用酒精灯加热 |
| B、把鼻孔凑近瓶口闻药品的气味 |
| C、酒精灯用完后,可用嘴吹灭 |
| D、实验用剩的药品一般不能随意丢弃,也不放回原瓶,但实验剩余的金属钠必须放回原瓶 |
芳香烃是指( )
| A、分子里含有苯环的化合物 |
| B、分子组成符合CnH2n-6 通式的一类有机物 |
| C、分子里含有一个或多个苯环的烃 |
| D、苯和苯的同系物的总称 |
下列反应不能通过一步反应得到的是( )
| A、Na2CO3→NaHCO3 |
| B、SiO2→H2SiO3 |
| C、Fe(OH)2→Fe(OH)3 |
| D、NH4Cl→NH3 |
以NA表示阿佛加德罗常数,下列说法中正确的是( )
| A、53g碳酸钠中含NA个CO32- |
| B、标准状况下11.2L臭氧中含NA个氧原子 |
| C、1.8g水中含NA个中子 |
| D、0.1molOH-含NA个电子 |
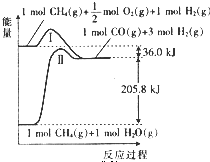 合成气(CO和H2为主的混合气体)不但是重要的燃料,也是重要的化工原料,图中曲线Ⅰ和Ⅱ是两种合成CO和H2反应的能量变化图.
合成气(CO和H2为主的混合气体)不但是重要的燃料,也是重要的化工原料,图中曲线Ⅰ和Ⅱ是两种合成CO和H2反应的能量变化图.