题目内容
20.在NaCl饱和溶液中通入HCl(g)时,NaCl(s)能沉淀析出的原因是( )| A. | HCl水溶液是强酸,任何强酸都导致有沉淀析出 | |
| B. | Cl-浓度增大,使平衡向生成氯化钠的方向移动,生成NaCl(s) | |
| C. | 酸的存在降低了Ksp(NaCl)的数值 | |
| D. | Ksp(NaCl)不受酸的影响,但增加Cl-浓度,能使Ksp(NaCl)减小 |
分析 饱和氯化钠溶液中存在NaCl(s)?Na+(aq)+Cl-(aq),通入HCl(g)时,氯离子浓度增大,结合平衡移动解答.
解答 解:饱和氯化钠溶液中存在NaCl(s)?Na+(aq)+Cl-(aq),通入HCl(g)时,氯离子浓度增大,则溶解平衡逆向移动,所以沉淀析出,但Ksp(NaCl)不变,故选B.
点评 本题主要考查溶解平衡移动,把握溶解平衡及氯离子对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列叙述不正确的是( )
| A. | CH4与C4H10互为同系物 | |
| B. | C5H12有三种同分异构体 | |
| C. | 乙烯、乙醇和乙酸都可以使高锰酸钾溶液褪色 | |
| D. | 苯分子中的碳碳键是介于单键和双键之间的独特的键 |
8.在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表,
关于此反应的认识正确的是( )
关于此反应的认识正确的是( )
| 物质 | W | G | H | P |
| 反应前质量/g | 20 | 2 | 1 | 37 |
| 反应后质量/g | a | 32 | 1 | 12 |
| A. | a=5 | B. | H一定是该反应的催化剂 | ||
| C. | 该反应是化合反应 | D. | 在反应中,G、P的质量比为8:3 |
5.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=3的溶液中:Na+、NO3-、Fe2+、SO42- | |
| B. | 加入铝粉能产生氢气的溶液中:NH4+、CH3COO-、SO42-、NO3- | |
| C. | 某酸性溶液中Na+、ClO?、SO42?、I? | |
| D. | 在0.1mol•L-1 AlC13溶液中:H+、Na+、Cl-、NO3- |
12.常温下,下列说法正确的是( )
| A. | 0.1 mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A) | |
| B. | 等体积、等物质的量浓度的NaCl(aq) 微粒种类大于NaClO(aq)中微粒种类 | |
| C. | pH=3的硫酸溶液中水的电离程度大于pH=11的氨水溶液中水的电离程度 | |
| D. | 体积相同的0.1 mol/L氨水和0.1 mol/L NaOH溶液中和盐酸的能力后者大 |
9.现有四份体积、浓度均相等的AgNO3溶液,分别与等物质的量浓度的下列溶液恰好完全反应,所需溶液体积最小的是( )
| A. | ZnCl2溶液 | B. | NaCl溶液 | C. | CaCl2溶液 | D. | AlCl3溶液. |
10.下列有关说法正确的是( )
| A. | 配制Fe(NO3)2溶液时,为了防止Fe2+水解可向溶液中加入适量的稀硝酸 | |
| B. | 向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,则Ksp(BaCO3)<Ksp(BaSO4) | |
| C. | pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 | |
| D. | 已知I2可溶于KI形成KI3,向两支盛有KI3溶液的试管中,分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀,说明KI3溶液中存在平衡:I3-?I2+I- |

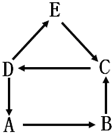 A、B、C、D、E为初中化学常见物质,A是单质,其余为化合物.E可用于检验气体B,它们之间有如图所示的转化关系(“→”表示生成,部分反应物、生成物、反应条件已省略).回答下列问题:
A、B、C、D、E为初中化学常见物质,A是单质,其余为化合物.E可用于检验气体B,它们之间有如图所示的转化关系(“→”表示生成,部分反应物、生成物、反应条件已省略).回答下列问题: