题目内容
下表是元素周期表的一部分,根据所给的10种元素,完成以下各小题.
(1)化学性质最不活泼的元素是 (填元素符号).
(2)镁的原子结构示意图为 .
(3)N与O原子半径较大的是 .
(4)H2SO4与HClO4中,酸性较强的是 .
(5)NaOH与Al(OH)3中,属于两性氢氧化物的是 ,它常用作治疗胃酸(含盐酸)过多的药物,该反应的离子方程式为 .
(6)Si是良好的半导体材料,它的氧化物常用于制造 (填一种高性能的现代通讯材料).
(7)碳元素形成的一种氧化物的化学式是 ,该物质中C元素与O元素的质量比为 .(相对原子质量:C-12 O-16)
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)镁的原子结构示意图为
(3)N与O原子半径较大的是
(4)H2SO4与HClO4中,酸性较强的是
(5)NaOH与Al(OH)3中,属于两性氢氧化物的是
(6)Si是良好的半导体材料,它的氧化物常用于制造
(7)碳元素形成的一种氧化物的化学式是
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:(1)稀有气体原子最外层为稳定结构,化学性质最不活泼;
(2)Mg原子核外有12个电子,有3个电子层,各层电子数为2、8、2;
(3)同周期自左而右原子半径减小;
(4)元素非金属性越强,其最高价氧化物对应水化物的酸性越强;
(5)氢氧化铝属于两性氢氧化物,胃酸主要成份为盐酸,氢氧化铝与盐酸反应生成氯化铝与水;
(6)二氧化硅可以用作光导纤维;
(7)碳的氧化物为CO或CO2,根据化学式确定元素质量之比.
(2)Mg原子核外有12个电子,有3个电子层,各层电子数为2、8、2;
(3)同周期自左而右原子半径减小;
(4)元素非金属性越强,其最高价氧化物对应水化物的酸性越强;
(5)氢氧化铝属于两性氢氧化物,胃酸主要成份为盐酸,氢氧化铝与盐酸反应生成氯化铝与水;
(6)二氧化硅可以用作光导纤维;
(7)碳的氧化物为CO或CO2,根据化学式确定元素质量之比.
解答:
解:(1)稀有气体Ne原子最外层有8个电子,为稳定结构,化学性质最不活泼,故答案为:Ne;
(2)Mg原子核外有12个电子,有3个电子层,各层电子数为2、8、2,原子结构示意图为: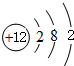 ,故答案为:
,故答案为: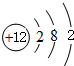 ;
;
(3)同周期自左而右原子半径减小,故原子半径N>O,故答案为:N;
(4)同周期自左而右元素非金属性减弱,故非金属性S<Cl,元素非金属性越强,其最高价氧化物对应水化物的酸性越强,故酸性HClO4>H2SO4,故答案为:HClO4;
(5)氢氧化铝属于两性氢氧化物,胃酸主要成份为盐酸,氢氧化铝与盐酸反应生成氯化铝与水,反应离子方程式为:Al(OH)3+3H+=Al3++3H2O,故答案为:Al(OH)3;Al(OH)3+3H+=Al3++3H2O;
(6)二氧化硅在高性能的现代通讯材料中可以用作光导纤维,故答案为:光导纤维;
(7)碳的氧化物为CO或CO2,由化学式可知C、O元素质量之比=12:16=3:4或C、O元素之比=12:32=3:8,
故答案为:CO或CO2;3:4或3:8.
(2)Mg原子核外有12个电子,有3个电子层,各层电子数为2、8、2,原子结构示意图为:
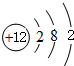 ,故答案为:
,故答案为: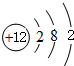 ;
;(3)同周期自左而右原子半径减小,故原子半径N>O,故答案为:N;
(4)同周期自左而右元素非金属性减弱,故非金属性S<Cl,元素非金属性越强,其最高价氧化物对应水化物的酸性越强,故酸性HClO4>H2SO4,故答案为:HClO4;
(5)氢氧化铝属于两性氢氧化物,胃酸主要成份为盐酸,氢氧化铝与盐酸反应生成氯化铝与水,反应离子方程式为:Al(OH)3+3H+=Al3++3H2O,故答案为:Al(OH)3;Al(OH)3+3H+=Al3++3H2O;
(6)二氧化硅在高性能的现代通讯材料中可以用作光导纤维,故答案为:光导纤维;
(7)碳的氧化物为CO或CO2,由化学式可知C、O元素质量之比=12:16=3:4或C、O元素之比=12:32=3:8,
故答案为:CO或CO2;3:4或3:8.
点评:本题考查元素周期律、元素化合物性质等,比较基础,注意对元素周期律的理解掌握.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相等(不考虑水解),且SO42-的物质的量浓度为9mol/L,则此溶液最多溶解Mg的质量为( )
| A、24g | B、18g |
| C、21.6g | D、14.4g |
下列关于电解质溶液的叙述中正确的是( )
| A、Na2CO3、NaHCO3两种盐的溶液中,离子种类不相同 |
| B、常温下1mol?L-1的CH3COOH溶液与1mol?L-1的NaOH溶液等体积混合,所得混合液中[Na+]>[CH3COO-]>[H+]>[OH-] |
| C、物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,[NH4+]前者小于后者 |
| D、常温下,某溶液中由水电离出的[H+]为1.0×10-5mol?L-1,则此溶液可能是盐酸,也可能是NH4Cl溶液 |
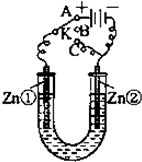 在一个U形管里盛有氯化铜溶液,并插入两块纯锌片作电极,如图所示:
在一个U形管里盛有氯化铜溶液,并插入两块纯锌片作电极,如图所示: 已知A、B、C、D四种短周期元素.在元素周期表中的相对位置如下图所示,其中B元素的氧化物是形成酸雨的主要成分.请填空:
已知A、B、C、D四种短周期元素.在元素周期表中的相对位置如下图所示,其中B元素的氧化物是形成酸雨的主要成分.请填空: