题目内容
【题目】25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
A.0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl﹣)>c(CH3COO﹣)>c(OH﹣)
B.0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7):c(NH3H2O)>c(NH4+)>c(Cl﹣)>c(OH﹣)
C.0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合: ![]() c(Na+)=c(CO32﹣)+c(HCO3﹣)+c(H2CO3)
c(Na+)=c(CO32﹣)+c(HCO3﹣)+c(H2CO3)
D.0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42﹣)+c(HC2O4﹣)+c(OH﹣)=c(Na+)+c(H+)
【答案】A
【解析】A、0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合反应生成NaCl和CH3COOH,醋酸是弱电解质存在电离平衡,溶液呈酸性,溶液中离子浓度c(Na+)=c(Cl﹣)>c(CH3COO﹣)>c(OH﹣),所以A正确; B、0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7),说明溶液中一水合氨电离大于铵根离子水解溶液呈碱性,c(NH4+)>c(Cl﹣)>c(NH3H2O)>c(OH﹣),所以B错误;
C、0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:n(Na):n(C)=3:2,溶液中物料守恒得到:2c(Na+)=3[c(CO32﹣)+c(HCO3﹣)+c(H2CO3)],所以C错误;
D、0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸)反应生成氯化钠、NaHC2O4 , 溶液中存在电荷守恒为:c(Cl﹣)+2c(C2O42﹣)+c(HC2O4﹣)+c(OH﹣)=c(Na+)+c(H+),所以D错误;所以选A.

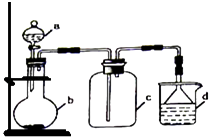
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略了净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 氯化铵 | NaOH | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
A.A
B.B
C.C
D.D