题目内容
8.在如图所示的转化关系中,括号内编号①-④表示转化所需化学试剂:
(1)用化学式填空:①是NaHCO3、②是NaOH或Na2CO3、③是Na、④是CO2(H2O)、
(2)A的结构简式是
 .
.(3)写出①反应生成A的化学方程式为
 +NaHCO3→
+NaHCO3→ +H2O+CO2↑.
+H2O+CO2↑.
分析 由图中官能团变化可知,①中只有-COOH转化为-COONa,则需要试剂为碳酸氢钠,②中酚-OH转化为酚钠,则需要试剂为碳酸钠或NaOH,③中醇-OH转化为-ONa,需要试剂为Na,④中酚钠转化为酚,需要试剂为二氧化碳,以此来解答.
解答 解:由图中官能团变化可知,①中只有-COOH转化为-COONa,则需要试剂为碳酸氢钠,②中酚-OH转化为酚钠,则需要试剂为碳酸钠或NaOH,③中醇-OH转化为-ONa,需要试剂为Na,④中酚钠转化为酚,需要试剂为二氧化碳,
(1)由上述分析可知,①中试剂为NaHCO3,②中试剂为NaOH或Na2CO3,③中试剂为Na,④中试剂为CO2(H2O),
故答案为:NaHCO3;NaOH或Na2CO3;Na;CO2(H2O);
(2)①中只有-COOH转化为-COONa,可知A为 ,故答案为:
,故答案为: ;
;
(3)①反应生成A的化学方程式为 +NaHCO3→
+NaHCO3→ +H2O+CO2↑,故答案为:
+H2O+CO2↑,故答案为: +NaHCO3→
+NaHCO3→ +H2O+CO2↑.
+H2O+CO2↑.
点评 本题考查有机物的推断及结构与性质,为高频考点,把握官能团的变化、发生的反应为解答本题关键,侧重分析与应用能力的考查,注意酚、醇、羧酸性质的应用,题目难度不大.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
13.一种盐X与烧碱混合共热,可放出无色气体Y,Y经一系列氧化后的产物再溶于水可得Z溶液,Y和Z溶液反应又可生成X,则盐X是( )
| A. | NH4NO3 | B. | NH4Cl | C. | (NH4)2SO4 | D. | NH4HCO3 |
10.下列物质中,能导电的有①⑤,属于电解质的③④⑦⑩,属于非电解质的是②⑥⑨
①Cu ②液氨 ③AgCl ④NaC1晶体 ⑤硫酸溶液 ⑥干冰 ⑦BaSO4⑧金刚石 ⑨蔗糖 ⑩冰醋酸(纯CH3COOH)
①Cu ②液氨 ③AgCl ④NaC1晶体 ⑤硫酸溶液 ⑥干冰 ⑦BaSO4⑧金刚石 ⑨蔗糖 ⑩冰醋酸(纯CH3COOH)
3.下列关于微粒半径的叙述中,正确的是( )
| A. | 金属阳离子的半径大于它的原子半径 | |
| B. | 金属阳离子的半径小于它的原子半径 | |
| C. | 非金属阴离子的半径小于其原子半径 | |
| D. | 核外电子排布相同的不同微粒,核电荷数越大半径越小 |
13.某学生对SO2与漂粉精的反应进行实验探究:
(1)写出C12和Ca(OH)2制取漂粉精的化学方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(2)向水中持续通入SO2,未观察到白雾.推测现象i的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀.
①实验a目的是验证Cl2是否存在;
②由实验a、b不能判断白雾中含有HC1,理由是与硝酸酸化的AgNO3产生的白色沉淀也可能是Ag2SO4或Ag2SO3;
(3)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HC1,无明显变化.取上层清液,加入BaC12溶液,产生白色沉淀.则沉淀X中含有的物质是CaSO4
②用离子方程式解释现象iii中黄绿色褪去的原因:SO2+Cl2+2H2O=4H++SO42-+2Cl-.
(4)测定漂粉精有效成分的质量分数.称取2.000g漂粉精于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.2000mol•L-1 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点.反应原理为:3C1O-+I-═3C1-+IO3-IO3-+5I-+3H2O═6OH-+3I2
实验测得数据如下表所示.
该漂白粉中有效成分的质量分数为7.15%.
| 操作 | 现象 |
| 取适量漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝,后褪色 |
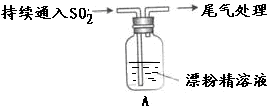 | 液面上方出现白雾; 稍后,出现浑浊,溶液变为黄绿色; 稍后,产生大量白色沉淀,黄绿色褪去 |
(2)向水中持续通入SO2,未观察到白雾.推测现象i的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀.
①实验a目的是验证Cl2是否存在;
②由实验a、b不能判断白雾中含有HC1,理由是与硝酸酸化的AgNO3产生的白色沉淀也可能是Ag2SO4或Ag2SO3;
(3)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HC1,无明显变化.取上层清液,加入BaC12溶液,产生白色沉淀.则沉淀X中含有的物质是CaSO4
②用离子方程式解释现象iii中黄绿色褪去的原因:SO2+Cl2+2H2O=4H++SO42-+2Cl-.
(4)测定漂粉精有效成分的质量分数.称取2.000g漂粉精于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.2000mol•L-1 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点.反应原理为:3C1O-+I-═3C1-+IO3-IO3-+5I-+3H2O═6OH-+3I2
实验测得数据如下表所示.
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
20.下列事实中,不能说明氯的非金属性比硫强的是( )
| A. | 高氯酸(HClO4)的酸性比硫酸强 | B. | 次氯酸的氧化性比稀硫酸强 | ||
| C. | 氯化氢比硫化氢的热稳定性好 | D. | 硫离子还原性比氯离子还原性强 |
17.有机化合物种类繁多的主要原因是( )
| A. | 有机化合物主要来自自然界众多的有机体 | |
| B. | 可以人工合成 | |
| C. | 有机物分子中的碳原子成键方式具有多样性 | |
| D. | 可以由无机物进行转化 |
18.元素性质随着原子序数的递增呈现周期性变化的根本原因是元素的( )
| A. | 原子的核外电子排布呈周期性变化 | B. | 原子半径呈周期性变化 | ||
| C. | 原子的电子层数呈周期性变化 | D. | 化合价呈周期性变化 |
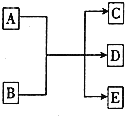 在一定条件下,物质A~E的转化关系如图所示,其中A为单质,常温下E为无色液体.
在一定条件下,物质A~E的转化关系如图所示,其中A为单质,常温下E为无色液体.