题目内容
乙烯的产量可用来衡量一个国家的石油化工发展水平.下列关于乙烯的说法不正确的是( )
| A、与苯互为同分异构体 |
| B、分子中存在碳碳双键 |
| C、能使溴的四氯化碳溶液褪色 |
| D、能使酸性高锰酸钾溶液褪色 |
考点:有机物的结构和性质,乙烯的化学性质
专题:有机化学基础
分析:乙烯为CH2=CH2,含碳碳双键,可发生加成、氧化反应,以此来解答.
解答:
解:A.乙烯为CH2=CH2,与苯(C6H6)的分子式不同,不是同分异构体,故A错误;
B.含碳碳双键,故B正确;
C.含双键,能使溴的四氯化碳溶液褪色,故C正确;
D.含双键,能使酸性高锰酸钾溶液褪色,故D正确;
故选A.
B.含碳碳双键,故B正确;
C.含双键,能使溴的四氯化碳溶液褪色,故C正确;
D.含双键,能使酸性高锰酸钾溶液褪色,故D正确;
故选A.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃性质的考查,注意CD中反应不同,题目难度不大.

练习册系列答案
 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
下列物质中属于电解质的是( )
①氢氧化钠 ②硫酸钡 ③铜 ④酒精 ⑤氯水.
①氢氧化钠 ②硫酸钡 ③铜 ④酒精 ⑤氯水.
| A、①② | B、①②⑤ | C、③④ | D、①⑤ |
在一定温度下,将气体X和气体Y 各0.16mol充入10L 恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A、反应前2min的平均速率v(Z)=0.04 mol/(L?min) |
| B、其他条件不变,升高温度,v(逆)增大,v(正)减小 |
| C、该温度下此反应的平衡常数K=1.44 |
| D、其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大 |
已知一定温度下,2X(g)+Y(g)?mZ(g)△H=-akJ/mol(a>0);现有甲、乙两容积相等且固定的密闭容器,在保持温度不变的情况下,向密闭容器甲中通入2molX和1molY,达到平衡状态时放出的热量为bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡状态时放出的热量为ckJ;且b>2c,则a、b、m的值或关系正确的是( )
| A、m=4 | B、a=b |
| C、a<b | D、m≤2 |
常温下,纯水中存在电离平衡:H2O?H++OH-.欲使水的电离平衡向正方向移动,并使c(H+)增大,应加入的物质是( )
| A、FeCl3 |
| B、H2SO4 |
| C、NaHCO3 |
| D、NaOH |
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列各项的事实不能说明上述观点的是( )
| A、甲苯能使酸性高锰酸钾溶液褪色,而苯不能使酸性高锰酸钾溶液褪色 |
| B、苯与硝酸发生反应生成硝基苯,甲苯与硝酸反应生成三硝基甲苯 |
| C、乙烯能发生加成反应,而乙烷不能发生加成反应 |
| D、苯酚中的羟基氢能与NaOH溶液反应,而醇羟基氢不能与NaOH溶液反应 |
上海作为2010年世博会的举办城市,公共交通的“绿色”也已经在进行,以二甲醚(化学式为C2H6O,简称甲醚)为燃料的公共交通作为“绿色”花园中的一点鲜艳的绿色已正式启动,解决了汽车尾部冒黑烟的问题.下列叙述正确的是( )
| A、甲醚与乙醇是同分异构体 |
| B、甲醚可由甲醇在一定条件下发生消去反应而制得 |
| C、甲醚作燃料不会产生氮的氧化物和碳氢化合物的污染 |
| D、1mol甲醚完全燃烧消耗的氧气与1mol甲醇完全燃烧消耗的氧气相同 |
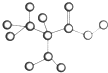 如图是某种只含有C、H、O、N的有机物简易球棍模型.请回答下列各题.
如图是某种只含有C、H、O、N的有机物简易球棍模型.请回答下列各题.