题目内容
砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等,氮、磷、砷位于同一主族,回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga As,第一电离能Ga As。(填“大于”或“小于”)
(3)氮原子的L层中有__________对成对电子,NH4+的立体构型是__________,其中心原子的杂化方式为__________;PCl3属于含有 键的 分子(填“极性”或“非极性”)。
练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
10.下列不能说明氯元素的非金属性比硫元素强的是( )
①HCl比H2S稳定
②HClO氧化性比H2SO4强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
①HCl比H2S稳定
②HClO氧化性比H2SO4强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
| A. | ①⑤ | B. | ② | C. | ①④ | D. | ①③⑤ |
吸热反应C+CO2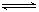 2CO反应速率为 ?1,放热反应N2+3H2
2CO反应速率为 ?1,放热反应N2+3H2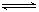 2NH3反应速率为 ?2,对于上述反应,当温度升高时,?1和
2NH3反应速率为 ?2,对于上述反应,当温度升高时,?1和 ?2的变化情况为? ?
?2的变化情况为? ?
A.同时增大  B.同时减小
B.同时减小
C.增大,减小 D.减小,增大
5.以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表,若混合溶液中Ca2+、Al3+、Fe3+的浓度均为1.0×10-3mol•L-1,c(AsO43-)最大是( )
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 5.7×10-21 |
| A. | 5.7×10-18 mol•L-1 | B. | 2.6×10-5mol•L-1 | ||
| C. | 1.6×10-13mol•L-1 | D. | 5.7×10-24mol•L-1 |


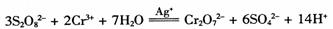 的反应速率与浓度的关系。反应速率v(Cr3+)可通过测定c(Cr3+)减半所需时间来确定。在一定温度下,获得如下实验数据:
的反应速率与浓度的关系。反应速率v(Cr3+)可通过测定c(Cr3+)减半所需时间来确定。在一定温度下,获得如下实验数据: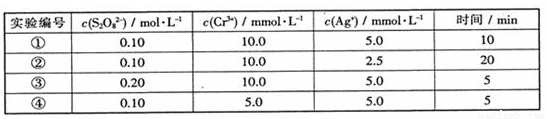
 误的是
误的是 液中溶质的物质的量浓度为2mol/L。
液中溶质的物质的量浓度为2mol/L。