题目内容
(每空1分,共6分)
写出除去下列物质中的杂质(括号内物质)所用的试剂,并写出发生的离子方程式。
(1)NaOH溶液(Na2CO3) , 。
(2)NaCl溶液(MgCl2) , 。
(3)KCl溶液(CuSO4) , 。
(每空1分,共6分)
(1)Ca(OH)2或Ba(OH)2 Ca2++CO32-=CaCO3↓或Ba2++CO32-=BaCO3↓
(2)NaOH Mg2++2OH-=Mg(OH)2↓
(3)Ba(OH)2 Cu2++SO42-+Ba2++2OH-=BaSO4↓+Mg(OH)2↓
【解析】
试题分析:除杂时除去原有的杂质,同时不能引入新的杂质。(1)NaOH溶液(Na2CO3),应选择适量的氢氧化钡或氢氧化钙溶液除去,氢氧化钡或氢氧化钙与碳酸根离子反应生成碳酸钡或碳酸钙沉淀,然后过滤除去,离子方程式是Ca2++CO32-=CaCO3↓或Ba2++CO32-=BaCO3↓;
(2)NaCl溶液(MgCl2),除去镁离子,应选择氢氧化物,但不能引入新的杂质,所以选择NaOH溶液,与镁离子反应生成氢氧化镁沉淀,离子方程式是Mg2++2OH-=Mg(OH)2↓;
(3)KCl溶液(CuSO4),铜离子应用氢氧化物除去,硫酸根离子用钡离子除去,二者结合应选择氢氧化钡溶液,氢氧化钡与硫酸铜反应生成氢氧化铜和硫酸钡沉淀,离子方程式是Cu2++SO42-+Ba2++2OH-=BaSO4↓+Mg(OH)2↓。
考点:考查物质的除杂试剂的判断,离子方程式的书写

(15分)某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体 g。
(2)配制过程中需要用到的玻璃仪器除烧杯、玻璃棒外还需要有 、 。
Ⅱ.测定中和热的实验装置如下图所示。
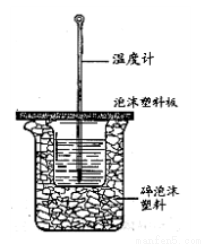
(3)大小烧杯之间填满碎泡沫塑料的作用是 ,从实验装置上看,图中缺少的一种玻璃仪器 。
(4)使用补全仪器后的装置进行实验,取50mL 0.25mol/L H2SO4溶液与50mL0.55 mol/L NaOH溶液在小烧杯中进行中和反应,实验数据如下表。
①请填写下表中的空白:
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | ℃ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②通过计算可得中和热△H = (精确到小数点后一位)
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是 。(填字母)
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(5)实验中若用60mL0.25mol·L-1H2SO4溶液跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”、“不相等”),所求中和热 (填“相等”、“不相等”);若用50mL0.50mol·L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会 (填“偏大”、“偏小”、“不受影响”)。
25 ℃时,弱酸的电离平衡常数如表所示,下列离子反应方程式错误的是
弱酸 | H2SO3 | HClO | H2CO3 |
Ka1 | 1.54×10-2 | 2.95×10-8 | 4.30×10-7 |
Ka2 | 1.02×10-7 |
| 5.61×10-11 |
A.氯水中加入少量NaHCO3粉末:HCO3- + H+ = H2O+CO2↑
B.NaAl(OH)4溶液中通入足量的CO2:Al(OH)4-+CO2 =Al(OH)3↓+ HCO3-
C.NaClO溶液中通入少量CO2:2ClO- +H2O+CO2 = CO32- + 2HClO
D.Na2CO3溶液中通入少量SO2:2 CO32-+ H2O+ SO2 = SO32-+2HCO3-
 2O3,此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是
2O3,此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是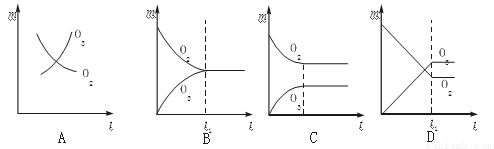
 H2O
H2O