题目内容
25 ℃时,弱酸的电离平衡常数如表所示,下列离子反应方程式错误的是
弱酸 | H2SO3 | HClO | H2CO3 |
Ka1 | 1.54×10-2 | 2.95×10-8 | 4.30×10-7 |
Ka2 | 1.02×10-7 |
| 5.61×10-11 |
A.氯水中加入少量NaHCO3粉末:HCO3- + H+ = H2O+CO2↑
B.NaAl(OH)4溶液中通入足量的CO2:Al(OH)4-+CO2 =Al(OH)3↓+ HCO3-
C.NaClO溶液中通入少量CO2:2ClO- +H2O+CO2 = CO32- + 2HClO
D.Na2CO3溶液中通入少量SO2:2 CO32-+ H2O+ SO2 = SO32-+2HCO3-
C
【解析】
试题分析:根据电离常数可知酸性强弱顺序是H2SO3>HSO3->H2CO3>HClO>HCO3-,则A.氯水中加入少量NaHCO3粉末只有元素与碳酸氢钠反应,即HCO3- + H+ = H2O+CO2↑,A正确;B.NaAl(OH)4溶液中通入足量的CO2生成氢氧化铝和碳酸氢钠,即Al(OH)4-+CO2 =Al(OH)3↓+ HCO3-,B正确;C.NaClO溶液中通入少量CO2生成次氯酸和碳酸氢钠,即ClO- +H2O+CO2 = HCO3- + HclO,C错误;D.Na2CO3溶液中通入少量SO2生成亚硫酸钠和碳酸氢钠,即2 CO32-+ H2O+ SO2 = SO32-+2HCO3-,D正确,答案选C。
考点:考查电离常数的应用

(8分)下图为长式周期表示意图,请根据A~G元素所在位置回答下列问题。
A |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| B | C | D |
|
|
E |
|
|
|
|
|
|
|
|
|
|
|
|
| F |
|
|
|
|
|
|
|
|
|
| G |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
注:答题时需将代号A~G替换为相应的元素符号
(1)元素A与C可形成两种分子C2A4与CA3,写出C2A4的结构式_______________。
(2)元素E与D能形成两种化合物E2D2与E2D,写出E2D2的电子式______________。
(3)元素A~G中,属于过渡元素的是_________。
(4)元素B、F的非金属性强弱关系为___________,设计实验验证此结论__________
________________________________________________________________________。
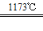 aTiCl4+eCO Ⅰ
aTiCl4+eCO Ⅰ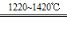 Ti+2MgCl2 Ⅱ
Ti+2MgCl2 Ⅱ B.丙烷分子的球棍模型:
B.丙烷分子的球棍模型: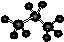
 D.原子核内有20个中子的氯原子:
D.原子核内有20个中子的氯原子: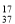 Cl
Cl