题目内容
根据下列要求回答相关问题:
(1)漂白粉的有效成分是 (填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是 (填化学式).写出工业上制备漂白粉的化学反应方程式
(2)根据化学物质的俗名写出它们的化学式:
①磁性氧化铁 ②铁红 ③苏打 ④小苏打
(3)进行蒸馏操作除了带铁圈的铁架台、带铁夹的铁架台、酒精灯、石棉网、温度计、冷凝管、牛角管、沸石,还需要的玻璃仪器有 、 .
(4)为除去粗盐中的Ca2+、Mg2+、SO
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐固体
滤液
精盐判断第③步BaCl2已过量的方法是 .
(1)漂白粉的有效成分是
(2)根据化学物质的俗名写出它们的化学式:
①磁性氧化铁
(3)进行蒸馏操作除了带铁圈的铁架台、带铁夹的铁架台、酒精灯、石棉网、温度计、冷凝管、牛角管、沸石,还需要的玻璃仪器有
(4)为除去粗盐中的Ca2+、Mg2+、SO
2- 4 |
称取粗盐固体
| 溶解 |
| ① |
| NaOH |
| ② |
| BaCl2 |
| ③ |
| Na2CO3 |
| ④ |
| 过滤 |
| ⑤ |
| 适量盐酸 |
| ⑥ |
| 蒸发、结晶、烘干 |
| ⑦ |
考点:粗盐提纯,根据化合价正确书写化学式(分子式),氯、溴、碘及其化合物的综合应用,间接加热的仪器及使用方法
专题:
分析:(1)漂白粉的有效成分是次氯酸钙,长期露置于空气中的漂白粉,变质生成碳酸钙;
(2)根据化学物质的俗名分析;
(3)根据蒸馏操作所需要的仪器进行分析;
(4)根据判断BaCl2的过量方法分析.
(2)根据化学物质的俗名分析;
(3)根据蒸馏操作所需要的仪器进行分析;
(4)根据判断BaCl2的过量方法分析.
解答:
解:(1)工业上常用廉价的石灰乳吸 收工业氯气尾气制得漂白粉,漂白粉的有效成分是次氯酸钙;长期露置于空气中的漂白粉,会和空气中的二氧化碳水反应生成碳酸钙和次氯酸,加稀盐酸后产生CO2;工业上制备漂白粉的化学反应方程式:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,
故答案为:Ca(ClO)2;CO2;2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O.
(2)根据化学物质的俗名分析,磁性氧化铁是四氧化三铁;铁红是氧化铁;苏打是碳酸钠;小苏打是碳酸氢钠;
故答案为:Fe3O4、Fe2O3、Na2CO3、NaHCO3;
(3)进行蒸馏操作除了带铁圈的铁架台、带铁夹的铁架台、酒精灯、石棉网、温度计、冷凝管、牛角管、沸石,还需要的玻璃仪器有蒸馏烧瓶,锥形瓶;
故答案为:蒸馏烧瓶,锥形瓶;
(4)判断第③步BaCl2已过量的方法是静置,向上层清液中继续滴加少量BaCl2溶液,若无沉淀产生,则证明沉淀已完全;
故答案为:静置,向上层清液中继续滴加少量BaCl2溶液,若无沉淀产生,则证明沉淀已完全.
故答案为:Ca(ClO)2;CO2;2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O.
(2)根据化学物质的俗名分析,磁性氧化铁是四氧化三铁;铁红是氧化铁;苏打是碳酸钠;小苏打是碳酸氢钠;
故答案为:Fe3O4、Fe2O3、Na2CO3、NaHCO3;
(3)进行蒸馏操作除了带铁圈的铁架台、带铁夹的铁架台、酒精灯、石棉网、温度计、冷凝管、牛角管、沸石,还需要的玻璃仪器有蒸馏烧瓶,锥形瓶;
故答案为:蒸馏烧瓶,锥形瓶;
(4)判断第③步BaCl2已过量的方法是静置,向上层清液中继续滴加少量BaCl2溶液,若无沉淀产生,则证明沉淀已完全;
故答案为:静置,向上层清液中继续滴加少量BaCl2溶液,若无沉淀产生,则证明沉淀已完全.
点评:本题考查了氯气及其化合物性质的应用、物质的俗称、蒸馏、食盐的提纯,掌握各物质的性质是解题的关键.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
除去下列物质中所含少量杂质(括号内为杂质),所选用试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 乙烯(二氧化硫) | 溴水 | 洗气 |
| B | 溴苯(溴) | NaOH溶液 | 分液 |
| C | 苯(甲苯) | 酸性KMnO4溶液 | 过滤 |
| D | 乙烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
| A、A | B、B | C、C | D、D |
以下说法不正确的是( )
| A、甲烷的取代反应的条件是在光照条件下与卤素气态单质 |
| B、乙烯与卤素加成的条件是卤素单质的水溶液 |
| C、乙烯与酸性高锰酸钾的反应是加成反应 |
| D、苯的取代反应条件是液溴加催化剂 |
下列物质中,可用重结晶法提纯的是( )
| A、含杂质的粗苯甲酸 |
| B、含杂质的工业酒精 |
| C、从溴水中提纯溴 |
| D、苯中混有少量苯酚 |
下列不能直接用乙烯为原料制取的物质是( )
| A、CH3CH2Cl |
| B、CH2Cl-CH2Cl |
C、 |
D、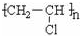 |
锌跟过量的2mol?L-1的盐酸反应,为加快反应速率,又不影响产生氢气的总量,可采用的方法是( )
| A、加入数滴氯化铜溶液 |
| B、加入适量的6mol?L-1的硝酸 |
| C、加入适量的2mol?L-1的硫酸 |
| D、加入适量的氯化钠溶液 |