题目内容
下列关于电解质溶液的叙述中正确的是( )
| A、Na2CO3、NaHCO3两种盐的溶液中,离子种类不相同 |
| B、常温下1mol?L-1的CH3COOH溶液与1mol?L-1的NaOH溶液等体积混合,所得混合液中[Na+]>[CH3COO-]>[H+]>[OH-] |
| C、物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,[NH4+]前者小于后者 |
| D、常温下,某溶液中由水电离出的[H+]为1.0×10-5mol?L-1,则此溶液可能是盐酸,也可能是NH4Cl溶液 |
考点:盐类水解的应用,弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:A.碳酸钠溶液中存在CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-、H2O?H++OH-,碳酸氢钠溶液中存在HCO3-=CO32-+H+、HCO3-+H2O?H2CO3+OH-、H2O?H++OH-;
B.二者恰好反应生成醋酸钠,醋酸钠为强碱弱酸盐,其溶液呈碱性;
C.氢离子抑制铵根离子水解;
D.常温下,某溶液中由水电离出的[H+]为1.0×10-5mol?L-1>1.0×10-7mol?L-1,说明溶质促进水电离,溶液呈酸性,则溶质为强酸弱碱盐.
B.二者恰好反应生成醋酸钠,醋酸钠为强碱弱酸盐,其溶液呈碱性;
C.氢离子抑制铵根离子水解;
D.常温下,某溶液中由水电离出的[H+]为1.0×10-5mol?L-1>1.0×10-7mol?L-1,说明溶质促进水电离,溶液呈酸性,则溶质为强酸弱碱盐.
解答:
解:A.碳酸钠溶液中存在CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-、H2O?H++OH-,碳酸氢钠溶液中存在HCO3-=CO32-+H+、HCO3-+H2O?H2CO3+OH-、H2O?H++OH-,所以两种溶液中离子种类相同,故A错误;
B.二者恰好反应生成醋酸钠,醋酸钠为强碱弱酸盐,其溶液呈碱性,则[H+]<[OH-],故B错误;
C.氢离子抑制铵根离子水解,所以氯化铵水解程度大于硫酸氢铵水解程度,则[NH4+]前者小于后者,故C正确;
D.常温下,某溶液中由水电离出的[H+]为1.0×10-5mol?L-1>1.0×10-7mol?L-1,说明溶质促进水电离,溶液呈酸性,则溶质为强酸弱碱盐,可能为氯化铵,故D错误;
故选C.
B.二者恰好反应生成醋酸钠,醋酸钠为强碱弱酸盐,其溶液呈碱性,则[H+]<[OH-],故B错误;
C.氢离子抑制铵根离子水解,所以氯化铵水解程度大于硫酸氢铵水解程度,则[NH4+]前者小于后者,故C正确;
D.常温下,某溶液中由水电离出的[H+]为1.0×10-5mol?L-1>1.0×10-7mol?L-1,说明溶质促进水电离,溶液呈酸性,则溶质为强酸弱碱盐,可能为氯化铵,故D错误;
故选C.
点评:本题考查了盐类水解,根据盐的特点判断溶液中存在的平衡、溶液酸碱性,易错选项是D,只有含有弱离子的盐才能促进水电离,酸或碱抑制水电离,为易错点.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
下列离子方程式错误的是( )
| A、小苏打溶液中加入过量的烧碱溶液:HCO3-+OH-=CO32-+H2O |
| B、澄清石灰水中通入过量的CO2:CO2+OH-=HCO3- |
| C、Cl2与水反应生成盐酸和次氯酸Cl2+H2O=2H++Cl-+ClO- |
| D、硫酸与氢氧化钡溶液反应:2H++2OH-+Ba2++SO42-=2H2O+BaSO4↓ |
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 用如图所示装置进行稀硝酸与铜的反应制取并收集NO |
B、 用如图所示装置进行用已知浓度的氢氧化钠溶液测定盐酸浓度的实验 |
C、 用如图所示装置制取少量Cl2 |
D、 用如图所示装置检验电流的方向 |
“保护环境,就是保护人类自己.”下列环境问题与产生的主要原因不相符的是( )
①“臭氧空洞”主要是大量使用氟氯代烃等引起的
②“光化学烟雾”主要是由NO2等引起的
③“酸雨”主要是由空气中CO2浓度增大引起的
④“白色污染”主要是由聚苯乙烯塑料等引起的
⑤“温室效应”主要是由空气中CO2浓度增大引起的
⑥“赤潮”主要是由水体中P、N等元素过量引起的.
①“臭氧空洞”主要是大量使用氟氯代烃等引起的
②“光化学烟雾”主要是由NO2等引起的
③“酸雨”主要是由空气中CO2浓度增大引起的
④“白色污染”主要是由聚苯乙烯塑料等引起的
⑤“温室效应”主要是由空气中CO2浓度增大引起的
⑥“赤潮”主要是由水体中P、N等元素过量引起的.
| A、只有①② | B、只有②③⑤ |
| C、全部 | D、只有③ |
在一定条件下,下列转化不能通过一步反应实现的是( )
| A、HCl→NaCl |
| B、CO→CaCO3 |
| C、Fe→FeSO4 |
| D、Ca(OH)2→NaOH |
有机物H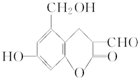 中不含有的官能团是( )
中不含有的官能团是( )
 中不含有的官能团是( )
中不含有的官能团是( )| A、醇羟基 | B、羧基 | C、醛基 | D、酯基 |
将磁性氧化铁放入稀HNO3中可发生如下反应:3Fe3O4+28HNO3=9Fe(NO3)x+NO↑+14H2O,下列判断合理的是( )
| A、Fe(NO3)x中的x为2 |
| B、稀HNO3在反应中只表现氧化性 |
| C、磁性氧化铁中的所有铁元素全部被氧化 |
| D、反应中每还原0.3mol氧化剂,就有0.9mol电子转移 |