题目内容
实验室用铅蓄电池作电源电解饱和食盐水制取Cl2,已知铅蓄电池放电时发生如下反应:
负极:Pb+SO42—-2e-=PbSO4
正极:PbO2+4H++SO42—+2e-=PbSO4+2H2O
今欲制得Cl2 0.050 mol, 这时电池内消耗的H2SO4的物质的量至少是( )。
负极:Pb+SO42—-2e-=PbSO4
正极:PbO2+4H++SO42—+2e-=PbSO4+2H2O
今欲制得Cl2 0.050 mol, 这时电池内消耗的H2SO4的物质的量至少是( )。
| A.0.025 mol | B.0.050 mol | C.0.10 mol | D.0.20 mol |
C
要求得硫酸的量,需首先找出铅蓄电池的总反应。将上述两个电极反应合并可得:Pb+PbO2+2H2SO4=2PbSO4+2H2O。而在制取Cl2时,每生成1 mol Cl2,电子转移2 mol,现需要转移电子0.050 mol×2=0.100 mol。由铅蓄电池总反应可知,每转移0.100 mol电子,将消耗0.100 mol硫酸。

练习册系列答案
相关题目
 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当 铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答 下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当 铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答 下列问题。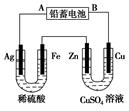
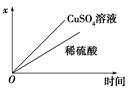
 2ZnO,下列判断正确的是( )
2ZnO,下列判断正确的是( )

 (1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为