题目内容
7.25℃时,在20mL0.1mol/L盐酸溶液中逐滴加入0.2mol/L氨水,曲线如图所示,下列说法正确的是( )
| A. | 此滴定实验可以选用酚酞做指示剂 | B. | 在A点:c(Cl-)>c(H+)>c(NH4+)>c(OH-) | ||
| C. | 在B点:c(H+)=c(OH-)=c(Cl-)=c(NH4+) | D. | 在C点:c(NH4+)+c(NH3•H2O)=2c(Cl-) |
分析 A.由于反应后的溶液溶质为氯化铵,溶液呈酸性,酚酞的变色范围为8.2-10.0,误差较大;
B.在A点,溶液呈酸性,由电荷守恒得c(Cl-)+c(OH-)=c(H+)+c(NH4+)分析;
C.在B点:溶液呈中性,所以c(H+)=c(OH-),溶液中存在电荷守恒,即c(Cl-)+c(OH-)=c(H+)+c(NH4+);
D.在C点,氨水的物质的量是盐酸物质的量的2倍,根据物料守恒判断.
解答 解:A.由于反应后的溶液溶质为氯化铵,溶液呈酸性,选择指示剂变色范围在酸性范围的甲基橙,而酚酞的变色范围为8.2-10.0,误差较大,故A错误;
B.在A点,溶液呈酸性,c(H+)>c(OH-),由电荷守恒得c(Cl-)+c(OH-)=c(H+)+c(NH4+),所以c(Cl-)>c(NH4+),根据图象知,溶液的pH接近7,所以溶液中c(NH4+)>c(H+),故B错误;
C.在B点:溶液呈中性,所以c(H+)=c(OH-),溶液中存在电荷守恒,即c(Cl-)+c(OH-)=c(H+)+c(NH4+),所以c(NH4+)=c(Cl-),但c(OH-)<c(Cl-),故C错误;D.在C点,氨水的物质的量是盐酸物质的量的2倍,根据物料守恒知,c(NH4+)+c(NH3.H2O)=2c(Cl-),故D正确;
故选D.
点评 本题考查酸碱的混合以及离子浓度的大小比较,题目难度中等,注意盐酸和氨水恰好完全反应时溶液不呈中性,要使溶液呈中性,氨水应稍微过量,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.有机化合物种类繁多的主要原因是( )
| A. | 有机化合物主要来自自然界众多的有机体 | |
| B. | 可以人工合成 | |
| C. | 有机物分子中的碳原子成键方式具有多样性 | |
| D. | 可以由无机物进行转化 |
18.元素性质随着原子序数的递增呈现周期性变化的根本原因是元素的( )
| A. | 原子的核外电子排布呈周期性变化 | B. | 原子半径呈周期性变化 | ||
| C. | 原子的电子层数呈周期性变化 | D. | 化合价呈周期性变化 |
15.下列化学用语的表达方式不正确的是( )
①乙酸乙酯的结构简式:CH3CH2COOCH2CH3
②CO2分子的结构式:O=C=O
③乙烯的实验式:CH2
④S原子的结构示意图: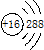
⑤葡萄糖结构简式:C6H12O6
⑥CH4Si的结构式:
①乙酸乙酯的结构简式:CH3CH2COOCH2CH3
②CO2分子的结构式:O=C=O
③乙烯的实验式:CH2
④S原子的结构示意图:
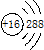
⑤葡萄糖结构简式:C6H12O6
⑥CH4Si的结构式:

| A. | 只有②⑤⑥ | B. | 只有①④⑤ | C. | 只有⑤⑥ | D. | 只有①②⑥ |
2.下列物质既不互为同系物也不互为同分异构体的是( )
| A. |  和 和 | B. |  和 和 | C. |  和 和 | D. |  和 和 |
19.若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化.在变化的各阶段被破坏的粒子间的主要相互作用依次是( )
| A. | 氢键 分子间作用力 非极性键 | |
| B. | 氢键 极性键 分子间作用力 | |
| C. | 氢键 氢键 极性键 | |
| D. | 分子间作用力 氢键 非极性键 |
17.有机化学中取代反应范畴很广,下列4个反应中,属于取代反应范畴的是( )
| A. | 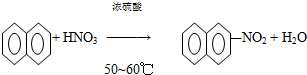 | |
| B. | CH3CH2CH2CHOHCH3$→_{△}^{浓硫酸}$CH3CH2CH=CHCH3+H2O | |
| C. | CH3CHO+H2$→_{催化剂}^{高温高压}$CH3CH2OH | |
| D. | 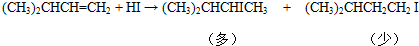 |

 .
.
 .
.